इलेक्ट्रोनएक्टिव्हिटी ही इतर घटकांच्या अणूपासून इलेक्ट्रॉनच्या अणूकडे इलेक्ट्रॉन आकर्षित करण्यासाठी असलेल्या रासायनिक घटकाची गुणधर्म आहे ज्यासह हे घटक संयुगे एक रासायनिक बंध बनवते.
जेव्हा वेगवेगळ्या घटकांच्या अणूंमध्ये एक रासायनिक बंध तयार होतो, तेव्हा सामान्य इलेक्ट्रॉन मेघ अधिक इलेक्ट्रोनॅगेटिव्ह अणूकडे वळतो, ज्यामुळे बॉन्ड सहानुभूती ध्रुवीय होते आणि इलेक्ट्रोनॅग्टीव्हिटीजमध्ये मोठ्या प्रमाणात फरक पडतो, आयनिक.
रासायनिक सूत्र लिहिताना इलेक्ट्रोनेगेटिव्हिटी विचारात घेतली जाते: बायनरी संयुगेमध्ये, सर्वात इलेक्ट्रोनॅगेटिव्ह घटकाचे प्रतीक मागे लिहिलेले असते.
इलेक्ट्रोनॅगेटीव्हिटी प्रत्येक कालखंडातील घटकांसाठी डावीकडून उजवीकडे वाढते आणि त्याच पीएस गटाच्या घटकांसाठी खाली वरून खाली कमी होते.
व्हॅलेन्स इतर अणूंच्या विशिष्ट संख्येसह एकत्रित करण्यासाठी घटक हा त्याच्या अणूंचा गुणधर्म आहे.
स्टोइचियोमेट्रिक, इलेक्ट्रॉनिक व्हॅलेन्स आणि समन्वय क्रमांक यांच्यात फरक करा. आम्ही केवळ स्टोचियोमेट्रिक व्हॅलेन्सचा विचार करू.
स्टोइचियोमेट्रिक व्हॅलेन्स दाखवते की या घटकाच्या अणूद्वारे दुसर्\u200dया घटकाचे किती अणू जोडलेले आहेत. व्हॅलेन्स युनिट हायड्रोजन व्हॅलेंस म्हणून घेतले जाते, तेव्हापासून हायड्रोजन नेहमीच मोनोव्हॅलेंट असतो. उदाहरणार्थ, एचसीएल, एच 2 ओ, एनएच 3 (अमोनिया एच 3 एनची शुद्ध शब्दलेखन आधीपासूनच आधुनिक मॅन्युअलमध्ये वापरली जाते), सीएच 4 क्लोरीन मोनोव्हॅलेंट आहे, ऑक्सिजन द्विगुणित आहे, नायट्रोजन क्षुल्लक आहे आणि कार्बन टेट्रॅव्हॅलेंट आहे.
ऑक्सिजनचे स्टोचिओमेट्रिक व्हॅलेन्स सहसा २ असते. बहुतेक सर्व घटक ऑक्सिजनसह संयुगे बनवतात, दुसर्या घटकाची मात्रा निश्चित करण्यासाठी मानक म्हणून ते वापरणे सोयीचे असते. उदाहरणार्थ, संयुगे ना 2 ओ, सीओओ, फे 2 ओ 3, एसओ 3 सोडियम मोनोव्हॅलेंट आहे, कोबाल्ट दिव्य आहे, लोह क्षुल्लक आहे, सल्फर हेक्साव्हॅलेंट आहे.
रेडॉक्स प्रतिक्रियांमध्ये, घटकांच्या ऑक्सिडेशन स्टेट्स निश्चित करणे आपल्यासाठी महत्त्वपूर्ण असेल.
ऑक्सिडेशन राज्य पदार्थातील घटकास त्याचे स्टोइचियोमेट्रिक व्हॅलेन्स असे म्हणतात, ते अधिक किंवा उणे चिन्हासह घेतले जाते.
रासायनिक घटक घटकांमध्ये विभागले जातात सतत वेलनेंस व्हेरिएबल व्हॅलेन्सचे घटक
1.3.3. आण्विक आणि अणु नसलेल्या रचनेचे पदार्थ. क्रिस्टल जाळीचा प्रकार. त्यांची रचना आणि रचना यावर पदार्थांच्या गुणधर्मांची अवलंबित्व.
निसर्गात असलेल्या यौगिकांच्या स्थितीनुसार ते आण्विक आणि अणु नसलेले विभागले गेले आहेत. IN आण्विक पदार्थ सर्वात लहान स्ट्रक्चरल कण रेणू आहेत. या पदार्थांमध्ये आण्विक क्रिस्टल जाली असते. अणु नसलेल्या पदार्थांमध्ये, सर्वात लहान स्ट्रक्चरल कण अणू किंवा आयन असतात. त्यांची क्रिस्टल जाळी अणू, आयनिक किंवा धातूसंबंधी आहे.
क्रिस्टल जाळीचा प्रकार मोठ्या प्रमाणात पदार्थांचे गुणधर्म ठरवते. उदाहरणार्थ, सह धातू क्रिस्टल जाळीचा धातूचा प्रकार, इतर सर्व घटकांपेक्षा भिन्न आहे उच्च प्लॅसिटी, इलेक्ट्रिकल आणि थर्मल चालकता... हे गुणधर्म, तसेच बरेच लोक - विकृती, धातू चमक इ. मेटल अणू दरम्यान विशेष प्रकारच्या बंधामुळे - धातू कनेक्शन हे लक्षात घ्यावे की धातूंमध्ये अंतर्भूत गुणधर्म केवळ कंडेन्डेड अवस्थेत दिसतात. उदाहरणार्थ, वायूमय अवस्थेतील चांदीमध्ये धातूंचे भौतिक गुणधर्म नसतात.
धातूंमध्ये एक विशेष प्रकारचे बंध - धातू - व्हॅलेन्स इलेक्ट्रॉनच्या कमतरतेमुळे होते, म्हणून ते धातूच्या संपूर्ण संरचनेत सामान्य असतात. धातूंच्या संरचनेचे सर्वात सोप्या मॉडेलने असे गृहित धरले की धातूंच्या क्रिस्टल जाळीमध्ये मुक्त इलेक्ट्रॉनांनी वेढलेल्या सकारात्मक आयन असतात, गॅस रेणूप्रमाणे इलेक्ट्रॉनची हालचाल अनागोंदीपणे होते. तथापि, असे मॉडेल गुणात्मकपणे धातूंच्या ब properties्याच गुणधर्मांचे स्पष्टीकरण देताना परिमाणवाचक पडताळणीमध्ये अपुरे असल्याचे दिसून येते. धातुच्या अवस्थेच्या सिद्धांताच्या पुढील विकासामुळे निर्मिती निर्माण झाली धातूंचा झोन सिद्धांत, जे क्वांटम मेकॅनिक्सच्या संकल्पनेवर आधारित आहे.
क्रिस्टल जाळीच्या नोड्समध्ये कॅशन्स आणि मेटल अणू असतात आणि इलेक्ट्रॉन क्रिस्टल जॅटीससह मुक्तपणे फिरतात.
धातूंची वैशिष्ट्यपूर्ण यांत्रिक मालमत्ता आहे प्लास्टिक, त्यांच्या क्रिस्टल्सच्या अंतर्गत संरचनेच्या वैशिष्ठ्यांमुळे. प्लॅस्टीसीटी बाह्य शक्तींच्या प्रभावाखाली असलेल्या शरीरात विकृती आणण्याची क्षमता समजली जाते, जे बाह्य प्रभावाच्या समाप्तीनंतरही कायम आहे. धातूंची ही मालमत्ता त्यांना फोर्जिंगच्या वेळी वेगवेगळ्या आकारात आकारू देते, पत्रकात गुंडाळतात किंवा वायरमध्ये ओढतात.
धातूंचा प्लॅस्टीसिटी या वस्तुस्थितीमुळे आहे की बाह्य प्रभावाखाली क्रिस्टल जाळी तयार होणा ्या आयनांचे थर फोडल्याशिवाय एकमेकांशी संबंधित आहेत. विस्थापित इलेक्ट्रॉन, मुक्त पुनर्वितरणामुळे, आयनिक थरांदरम्यान संवाद साधत राहतात या वस्तुस्थितीचा परिणाम म्हणून हे उद्भवते. अणू जाळी असलेल्या घन वर यांत्रिक कृती अंतर्गत, वैयक्तिक स्तर विस्थापित होतात आणि फुटण्यामुळे त्यामधील चिकटलेले तुकडे होतात सहसंयोजक बंध.
आयन, नंतर हे पदार्थ तयार होतात आयनिक प्रकारचे क्रिस्टल जाली.

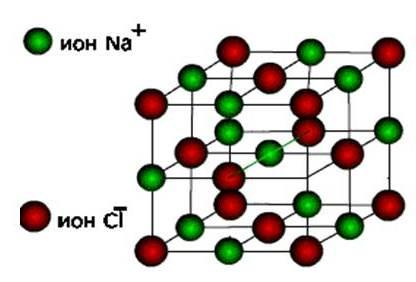
हे खारट पदार्थ, तसेच ऑक्सिडेज आणि ठराविक धातूंचे हायड्रोक्साइड्स आहेत. हे कठोर, नाजूक पदार्थ आहेत, परंतु त्यांची मुख्य गुणवत्ता आहे : या यौगिकांचे निराकरण आणि वितळणे विद्युतीय प्रवाह चालविते.
क्रिस्टल जाळीच्या साइट असल्यास अणू, नंतर हे पदार्थ तयार होतात अणू प्रकारची क्रिस्टल जाळी(डायमंड, बोरॉन, अॅल्युमिनियम आणि सिलिकॉनचे सिलिकॉन ऑक्साईड्स). पाण्यात अघुलनशील, गुणधर्मांमध्ये अतिशय कठोर आणि अपवर्तक
क्रिस्टल जाळीच्या साइट असल्यास रेणू, नंतर हे पदार्थ तयार होतात (सामान्य परिस्थितीत वायू आणि द्रव: О 2, एचसीएल; आय 2) सेंद्रिय पदार्थ).
धातूचे गॅलियम लक्षात घेणे मनोरंजक आहे, जे 30 डिग्री सेल्सियस तपमानावर वितळते हे विसंगती हे स्पष्ट करते की गा 2 रेणू क्रिस्टल जाळीच्या नोड्समध्ये स्थित आहेत आणि त्याचे गुणधर्म ज्यामध्ये आण्विक क्रिस्टल जाली असलेल्या पदार्थांसारखे बनतात.
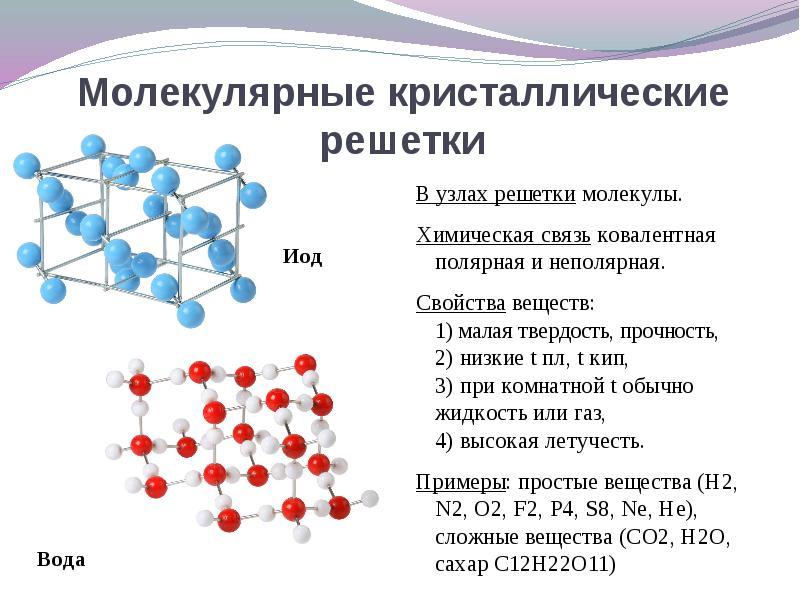
उदाहरण.गटाच्या सर्व धातू नसलेली रेणू नसलेली रचना असतेः
1) कार्बन, बोरॉन, सिलिकॉन; 2) फ्लोरीन, ब्रोमिन, आयोडीन;
3) ऑक्सिजन, सल्फर, नायट्रोजन; 4) क्लोरीन, फॉस्फरस, सेलेनियम
अणु नसलेल्या पदार्थांमध्ये, सर्वात लहान स्ट्रक्चरल कण अणू किंवा आयन असतात. त्यांची क्रिस्टल जाळी अणू, आयनिक किंवा धातूसंबंधी आहे
कधी निर्णय हा प्रश्न उलट्या पासून जाणे सोपे आहे. क्रिस्टल जाळीच्या साइट असल्यास रेणू, नंतर हे पदार्थ तयार होतात स्फटिक जाळीचा आण्विक प्रकार(सामान्य परिस्थितीत वायू आणि द्रवपदार्थ: ओ 2, एचसीएल; तसेच मी 2, गॉम्बिक सल्फर एस 8, पांढरा फॉस्फरस पी 4, सेंद्रिय पदार्थ). त्यांच्या गुणधर्मांनुसार, हे नाजूक लो-वितळणारे संयुगे आहेत.
दुसर्\u200dया उत्तरात फ्लोरिन गॅस आहे, तिसर्\u200dयामध्ये - ऑक्सिजन आणि नायट्रोजन वायू, चौथ्यामध्ये - क्लोरीन वायू. याचा अर्थ असा आहे की या पदार्थांमध्ये आण्विक क्रिस्टल जाली आणि आण्विक रचना आहे.
IN पहिला उत्तर असे आहे की सर्व पदार्थ सामान्य परिस्थितीत घन संयुगे असतात आणि एक अणु जाळी तयार करतात, ज्याचा अर्थ असा की त्यांच्यामध्ये आण्विक रचना नसते.
बरोबर उत्तरः1) कार्बन, बोरॉन, सिलिकॉन
- कमीतकमी इलेक्ट्रोनॅगेटिव्ह रासायनिक घटक आहे
- लोह
- मॅग्नेशियम
- कॅल्शियम
"कमीतकमी इलेक्ट्रोनॅजेटिव्ह" या वाक्यांकडे लक्ष दिले पाहिजे, म्हणजेच सर्वात मोठा धातूचा गुणधर्म असलेले घटक. या युक्तिवादानुसार आम्हाला संभाव्य उत्तरांमधून नायट्रोजन वगळण्याची अनुमती मिळेल, धातू नसलेली म्हणून, आणि कॅल्शियमवर रहा, कारण कार्यात प्रस्तावित केलेल्या धातुंपैकी सर्वात सक्रिय आहे. उत्तर: 4.
- रेणूंपैकी एकामधील सर्वात ध्रुवीय रासायनिक बंध
- सीसीएल 4
- सीबीआर 4
डीआय च्या नियतकालिक सारणीच्या कालावधी आणि गटांमधील इलेक्ट्रोनेगेटिव्हिटीमधील बदलांच्या नियमिततेबद्दल माहिती. उत्तरः २.
- हायड्रोजन क्लोराईड आणि क्लोरीनच्या रेणूंमध्ये अनुक्रमे रासायनिक बंध
- आयनिक आणि सहसंयोजक ध्रुवीय
- आयनिक आणि सहसंयोजक नॉन-ध्रुवीय
- सहसंयोजक ध्रुवीय आणि सहसंयोजक नॉन-ध्रुवीय
- हायड्रोजन आणि सहसंयोजक नॉन-पोलर
हे कार्य त्वरीत आणि योग्यरित्या पूर्ण करण्यासाठी मुख्य शब्द "त्यानुसार" आहे. प्रस्तावित रूपांमध्ये, उत्तरांपैकी केवळ एक उत्तर "कोव्हलेंट पोलर" या शब्दापासून सुरू होते, म्हणजेच हायड्रोजन क्लोराईडचे बंधन वैशिष्ट्य आहे. उत्तर: 3.
- कंपाऊंडमधील मॅंगनीझची ज्वलन स्थिती ज्यांचे सूत्र के 2 एमएनओ 4 आहे
सूत्राद्वारे घटकांच्या ऑक्सिडेशन स्टेट्सची गणना करण्याचे नियम जाणून घेतल्यास आपल्याला योग्य उत्तर निवडण्याची परवानगी मिळेल. उत्तर: 3.
- मीठातील सल्फरमध्ये ऑक्सिडेशनची स्थिती सर्वात कमी आहे
- पोटॅशियम सल्फेट
- पोटॅशियम सल्फाइट
- पोटॅशियम सल्फाइड
- पोटॅशियम हायड्रोजन सल्फेट
अर्थात, या कार्याची त्वरित पूर्तता करण्यात क्षाराची नावे सूत्रात अनुवाद करून दिली जाईल. गंधक हा गट व्हीआयएचा घटक असल्याने, त्याची सर्वात कमी ऑक्सीकरण स्थिती -2 आहे. हे मूल्य के 2 एस - पोटॅशियम सल्फाइड सूत्राच्या संयुगेशी संबंधित आहे. उत्तर: 3.
- ऑक्सीकरण स्थिती +5 क्लोरीन अणू आयनमध्ये असते
- सी 1 ओ - 4
- C1O -
- सी 1 ओ - 3
- सी 1 ओ - 2
हे कार्य पार पाडताना आपण या गोष्टीकडे लक्ष दिले पाहिजे की या स्थितीत विद्युतदृष्ट्या तटस्थ संयुगे दिली जात नाहीत, परंतु एकाच नकारात्मक शुल्कासह क्लोरीन आयन ("-") दिले पाहिजेत. आयनमधील अणूंच्या ऑक्सिडेशनच्या जोडीची बेरीज आयनच्या शुल्काइतकीच असल्याने इच्छित आयनमधील ऑक्सिजन अणूंचे एकूण नकारात्मक शुल्क -6 (+5 - 6 \u003d -1) असावे. उत्तर: 3.
- ऑक्सिडेशन स्टेट -3 नायट्रोजन दोन संयुगे प्रत्येकामध्ये असते
- एनएफ 3 आणि एनएच 3
- एनएच 4 सीएल आणि एन 2 ओ 3
- एनएच 4 सीएल आणि एनएच 3
- एचएनओ 2 आणि एनएफ 3
योग्य उत्तर निश्चित करण्यासाठी, आपल्याला मानसिकरित्या उत्तर पर्याय डाव्या आणि उजव्या उप-स्तंभांमध्ये विभाजित करणे आवश्यक आहे. मग त्यापैकी एक निवडा ज्यामध्ये संयुगे एक सोपी रचना आहे - आमच्या बाबतीत, हे बायनरी संयुगेचे योग्य उप-स्तंभ आहे. विश्लेषणामुळे उत्तरे 2 आणि 4 वगळता येतील कारण ऑक्साईड आणि फ्लोराईड नायट्रोजनमध्ये कमी इलेक्ट्रोनॅजेटिव्ह घटकाप्रमाणे सकारात्मक ऑक्सीकरण स्थिती असते. हा युक्तिवाद आपल्याला उत्तर 1 वगळण्याची परवानगी देतो कारण त्यातील पहिला पदार्थ समान नायट्रोजन फ्लोराईड आहे. उत्तर: 3.
- पदार्थांना आण्विक रचना लागू करू नका
- कार्बन डाय ऑक्साइड
- मिथेन
- हायड्रोजन क्लोराईड
- कॅल्शियम कार्बोनेट
आपण असाइनमेंटच्या स्थितीत अंतर्भूत नकारात्मक निर्णयाकडे लक्ष दिले पाहिजे. सामान्य परिस्थितीत वायूयुक्त पदार्थांची घन अवस्थेत आण्विक क्रिस्टल जाली असते, त्यामुळे १- 1-3 पर्याय कार्य अटी पूर्ण करीत नाहीत. लवणांना कॅल्शियम कार्बोनेटची असाइनमेंट पुन्हा एकदा योग्य उत्तराची पुष्टी करेल. उत्तर: 4.
- पदार्थांचे गुणधर्म आणि त्यांची रचना याबद्दल खालील निर्णय योग्य आहेत का?
उत्तर: ओल्या लाँड्री दंव मध्ये कोरड्या पडतात कारण आण्विक रचनेचे पदार्थ उच्चशोटीसाठी (उच्च बनाने की क्रिया) करण्यास सक्षम असतात.
बी. ओले कपडे धुऊन मिळण्याचे प्रमाण थंडीत कोरडे होते कारण पाण्याचे रेणूंचे रेणूंचे वजन कमी असते.
- फक्त ए खरे आहे
- फक्त बी सत्य आहे
- दोन्ही निर्णय योग्य आहेत
- दोन्ही निर्णय योग्य नाहीत
ज्ञान भौतिक गुणधर्म आण्विक रचनेचे पदार्थ आम्हाला हे ठरविण्यास परवानगी देतात की थंडीत ओले कपडे वाळवण्यामागचे कारण म्हणजे बर्फाची उच्च क्षमता तयार करणे आणि पाण्याचे रेणूंची द्विध्रुवीय रचना नव्हे. उत्तरः १.
- प्रत्येक पदार्थाची आण्विक रचना असते, ज्याची सूत्रे मालिकेत दिली जातात
- सीओ 2, एचएनओ 3, सीओओ
- ना 2 एस, बीआर 2, क्रमांक 2
- एच 2 एसओ 4, क्यू, ओ 3
- एसओ 2, आय 2, एचसीएल
प्रस्तावित पर्यायांमध्ये प्रत्येकी तीन पदार्थ असतात, म्हणून या पर्यायांना मानसिकरित्या तीन उभ्या खांबांमध्ये विभाजित करणे तर्कसंगत आहे. त्यापैकी प्रत्येकाचे विश्लेषण, एक सोपी रचना (मध्यम स्तंभ) च्या पदार्थापासून प्रारंभ केल्याने उत्तर 3 दूर होईल, कारण त्यात तांबे धातू आहे, ज्यामध्ये मेटल क्रिस्टल जाळी आहे. उजव्या सब-कॉलमचे समान विश्लेषण आम्हाला उत्तर 1 वगळण्याची अनुमती देईल, कारण त्यात क्षारीय पृथ्वी मेटल ऑक्साईड (आयनिक लॅटीस) आहे. उर्वरित दोन पर्यायांमधून, पर्याय 2 वगळणे आवश्यक आहे, कारण त्यात एक क्षार मेटल मीठ आहे - सोडियम सल्फाइड (आयनिक लॅटीस). उत्तर: 4.
स्वत: ची अभ्यासाची कार्ये
- कंपाऊंडमध्ये ऑक्सिडेशन स्टेट +5 नायट्रोजन प्रदर्शित होते, ज्याचे सूत्र आहे
- एन 2 ओ 5
- एन 2 ओ 4
- एन 2 ओ
- ज्यांचे सूत्र (एनएच 4) 2 सीआर 2 ओ 7 आहे अशा कंपाऊंडमध्ये क्रोमियमची ऑक्सीकरण स्थिती
- नायट्रोजनची ऑक्सिडेशन स्टेट अनेक पदार्थांमध्ये कमी होते, ज्याची सूत्रे
- एनएच 3, क्रमांक 2, केएनओ 3
- एन 2 ओ 4, केएनओ 2, एनएच 4 सीएल
- एन 2, एन 2 ओ, एनएच 3
- एचएनओ 3, एचएनओ 2, क्रमांक 2
- क्लोरीनची ऑक्सिडेशन स्टेट अनेक पदार्थांमध्ये वाढते, ज्याची सूत्रे
- ,लो, आयएलओ 4, ऑलो 3
- 2l 2, С1 2 O 7, किंवा 3
- सीए (सी 1 ओ) 2, केसीएलओ 3, एचसीएलओ 4
- ,L, 3lO 3, OlO
- रेणूमधील सर्वात ध्रुवीय रासायनिक बंध
- अमोनिया
- हायड्रोजन सल्फाइड
- हायड्रोजन ब्रोमाइड
- हायड्रोजन फ्लोराईड
- सहसंयोजक नॉन-ध्रुवीय बंधनासह पदार्थ
- पांढरा फॉस्फरस
- अ\u200dॅल्युमिनियम फॉस्फाइड
- फॉस्फरस (व्ही) क्लोराईड
- कॅल्शियम फॉस्फेट
- केवळ आयनिक बाँड्स असलेल्या पदार्थांचे सूत्र सलग लिहिलेले आहेत
- सोडियम क्लोराईड, फॉस्फरस (व्ही) क्लोराईड, सोडियम फॉस्फेट
- सोडियम ऑक्साईड, सोडियम हायड्रॉक्साईड, सोडियम पेरोक्साईड
- कार्बन डायसल्फाईड, कॅल्शियम कार्बाईड, कॅल्शियम ऑक्साईड
- कॅल्शियम फ्लोराईड, कॅल्शियम ऑक्साईड, कॅल्शियम क्लोराईड
- अणू क्रिस्टल जाळी आहे
- सोडियम ऑक्साईड
- कॅल्शियम ऑक्साईड
- सल्फर (IV) ऑक्साईड
- अ\u200dॅल्युमिनियम ऑक्साईड
- आयनिक कनेक्शन क्रिस्टल जाळी क्लोरीनच्या परस्परसंवादाने स्थापना केली
- फॉस्फरस
- बेरियम
- हायड्रोजन
- राखाडी
- अमोनियम क्लोराईड बद्दल खालील निर्णय योग्य आहेत का?
ए. अमोनियम क्लोराईड - आयओनिक संरचनेचा एक पदार्थ, सहसंयोजक ध्रुवीय आणि आयनिक बंधांमुळे तयार झाला.
बी. अमोनियम क्लोराईड आयनिक रचनेचा एक पदार्थ आहे, आणि म्हणून घन, अपवर्तक आणि नॉन-अस्थिर
- फक्त ए खरे आहे
- फक्त बी सत्य आहे
- दोन्ही निर्णय योग्य आहेत
- दोन्ही निर्णय चुकीचे आहेत
08. इलेक्ट्रोनेगेटिव्हिटी, ऑक्सिडेशन स्टेट, ऑक्सिडेशन आणि कमी
रसायनशास्त्रात अस्तित्त्वात असलेल्या अत्यंत रंजक संकल्पनांच्या अर्थाविषयी चर्चा करूया आणि जसे विज्ञानात बर्\u200dयाचदा गोंधळात टाकणारे आणि उलटे वापरलेले आढळतात. आम्ही "इलेक्ट्रोनेगेटिव्हिटी", "ऑक्सिडेशन स्टेट" आणि "रेडॉक्स रिएक्शन" बद्दल बोलू.
याचा अर्थ काय आहे - संकल्पना उलथा वापरली जाते?
आम्ही हळूहळू त्याबद्दल सांगण्याचा प्रयत्न करू.
विद्युतप्रवाहता आम्हाला रासायनिक घटकाचे रेडॉक्स गुणधर्म दर्शविते. म्हणजेच विनामूल्य फोटॉन घेण्याची किंवा देण्याची त्याची क्षमता. आणि हा घटक ऊर्जा स्त्रोत किंवा शोषक (ईथर) आहे की नाही हे देखील. यांग किंवा यिन.
ऑक्सिडेशन राज्य इलेक्ट्रोनेगेटिव्हिटी सारखी संकल्पना आहे. हे घटकांच्या रेडॉक्स गुणधर्मांचे वैशिष्ट्य देखील दर्शवते. परंतु त्यांच्यात पुढील फरक आहे.
इलेक्ट्रोनॅगेटीव्हिटी एकल घटकाचे वैशिष्ट्य देते. स्वतःच, कोणत्याही रासायनिक संयुगेच्या संरचनेत शोधण्यापलीकडे. त्याच वेळी, ऑक्सिडेशन स्टेट त्याच्या रेडॉक्स क्षमतेचे वैशिष्ट्य ठरवते जेव्हा कोणत्याही रेणूच्या रचनेमध्ये घटक समाविष्ट केले जातात.
ऑक्सिडायझेशन करण्याची क्षमता काय आहे आणि पुनर्संचयित करण्याची क्षमता काय आहे याबद्दल थोडे बोलूया.
ऑक्सिडेशन विनामूल्य फोटॉन (इलेक्ट्रॉन) दुसर्\u200dया घटकाकडे हस्तांतरित करण्याची प्रक्रिया आहे. ऑक्सिडेशन मुळे इलेक्ट्रॉन काढून टाकणे अजिबात नाही, कारण आता विज्ञानात असा विश्वास आहे ... जेव्हा एखादा घटक दुसर्\u200dया घटकाचे ऑक्सिडाइझ करतो तेव्हा ते आम्ल किंवा ऑक्सिजन सारखे कार्य करते (म्हणूनच "ऑक्सिडेशन" असे नाव दिले जाते). ऑक्सिडायझिंग म्हणजे विनाश, क्षय, घटकांच्या ज्वलनास प्रोत्साहन देणे ... ऑक्सिडाईझ करण्याची क्षमता म्हणजे त्यांच्याद्वारे हस्तांतरित केलेल्या ऊर्जेद्वारे (फ्री फोटॉन) अणूंचा नाश करण्याची क्षमता. लक्षात ठेवा ऊर्जा नेहमीच वस्तू नष्ट करते.
विज्ञानाच्या तर्कशास्त्रात किती काळ विरोधाभास आहेत हे कोणालाही लक्षात आले नाही हे आश्चर्यकारक आहे.
उदाहरणार्थ: “आता आम्हाला माहित आहे की ऑक्सिडायझिंग एजंट हा एक पदार्थ आहे जो इलेक्ट्रॉन मिळवितो, आणि कमी करणारी एजंट म्हणजे पदार्थ जो त्यांना दूर करतो” (एका युवा रसायनशास्त्राचा विश्वकोश, लेख “रेडॉक्स रिएक्शन))”.
आणि आत्ताच खाली दोन परिच्छेद: "सर्वात मजबूत ऑक्सिडायझर विद्युत प्रवाह आहे (नकारात्मक चार्ज केलेल्या इलेक्ट्रॉनचा प्रवाह)" (आयबिड.).
त्या. पहिला कोट म्हणतो की ऑक्सिडंट म्हणजे इलेक्ट्रॉन स्वीकारतो, आणि दुसरा ऑक्सिडंट आहे जो सोडून देतो.
आणि अशा चुकीच्या, विरोधाभासी निष्कर्षांमुळे आपण शाळा आणि संस्थांमध्ये लक्षात ठेवू शकता!
हे ज्ञात आहे की सर्वोत्कृष्ट ऑक्सिडायझिंग एजंट हे धातू नसतात. शिवाय, पीरियड नंबर जितका लहान असेल तितक्या मोठ्या संख्येने आणि ऑक्सिडायझिंग एजंटची गुणधर्म अधिक स्पष्ट होईल. हे आश्चर्यकारक नाही. आम्ही नियतकाच्या रंगाच्या विषयी दुस talked्या भागात, नियतकालिक सारणीच्या विश्लेषणास समर्पित लेखात या कारणास्तव चर्चा केली. गट 1 ते 8 पर्यंत, घटकांमधील न्यूक्लियन्सचा रंग हळूहळू व्हायलेटपासून लालमध्ये बदलतो (जर आपण डी आणि एफ-घटकांचा निळा रंग देखील विचारात घेतला तर). पिवळ्या आणि लाल कणांचे संयोजन एकत्रित केलेले विनामूल्य फोटॉन्स सोडण्यास सुलभ करते. पिवळ्या जमतात, परंतु दुर्बलपणे टिकवून ठेवतात. आणि लाल लोकांचा परिणाम होण्यास हातभार लागतो. फोटॉन बंद करणे ही ऑक्सिडेशन प्रक्रिया आहे. परंतु जेव्हा काही लाल असतात, तेव्हा तेथे फोटॉन जमा करण्यास सक्षम कोणतेही कण नसतात. म्हणूनच गट 8 चे घटक, उदात्त वायू, ऑक्सिडायझिंग घटक नाहीत, त्यांच्या शेजार्\u200dयांप्रमाणेच, हॅलोजन.
पुनर्प्राप्ती ऑक्सीकरण विरूद्ध प्रक्रिया आहे. आजकाल विज्ञानात असे मानले जाते की जेव्हा एखाद्या रासायनिक घटकाला इलेक्ट्रॉन मिळतात तेव्हा ते कमी होते. हा दृष्टिकोन अगदी समजण्यायोग्य आहे (परंतु स्वीकारला गेला नाही) रासायनिक घटकांच्या संरचनेचा अभ्यास करताना असे आढळले की ते इलेक्ट्रॉन उत्सर्जित करतात. त्यांनी असा निष्कर्ष काढला की इलेक्ट्रॉन हा घटकांचा भाग असतो. याचा अर्थ असा आहे की एका घटकाकडे इलेक्ट्रॉनचे हस्तांतरण म्हणजे त्याच्या गमावलेल्या संरचनेची पुनर्संचयित करणे.
तथापि, प्रत्यक्षात, असे नाही.
इलेक्ट्रॉन हे विनामूल्य फोटॉन आहेत. ते न्यूक्लियन्स नाहीत. ते घटकांच्या शरीराचा भाग नाहीत. बाहेरून येणारे ते आकर्षित होतात आणि न्यूक्लियन्सच्या पृष्ठभागावर आणि त्या दरम्यान एकत्रित होतात. परंतु त्यांचे संचय एखाद्या घटकाची किंवा रेणूच्या पुनर्संचयित होण्यास अजिबातच जात नाही. उलटपक्षी, त्यांच्याद्वारे उत्सर्जित इथर (ऊर्जा) द्वारे केलेले हे फोटोन घटकांमधील बंध कमकुवत करतात आणि नष्ट करतात. आणि ही ऑक्सिडेशन प्रक्रिया आहे, परंतु घट नाही.
रेणू पुनर्संचयित करण्यासाठी, प्रत्यक्षात, त्यापासून ऊर्जा घेणे (या प्रकरणात, विनामूल्य फोटॉन), आणि संप्रेषण करणे नाही. फोटॉन घेऊन, कमी करणारे घटक पदार्थ घनरूप करते - ते पुनर्संचयित करते.
सर्वोत्तम कमी करणारे एजंट हे धातू आहेत. ही मालमत्ता नैसर्गिकरित्या त्यांच्या गुणात्मक आणि परिमाणात्मक रचना पासून येते - त्यांचे आकर्षण फील्ड सर्वात मोठे आहे आणि पृष्ठभागावर नेहमीच बरेच किंवा पुरेसे कण असतात निळ्या रंगाचे.
आपण धातूंची पुढील व्याख्या देखील काढू शकता.
धातू एक रासायनिक घटक आहे, ज्याच्या पृष्ठभागाच्या थरांमध्ये निळे कण असणे आवश्यक आहे.
ए धातू नसलेला - पृष्ठभागाच्या थरांच्या रचनामध्ये हे एक घटक आहे, ज्यामध्ये कोणतेही किंवा जवळजवळ कोणतेही निळे फोटॉन नाहीत आणि नेहमीच लाल असतात.
त्यांच्या मजबूत आकर्षणासह धातू इलेक्ट्रॉन पूर्णपणे काढून घेतात. आणि म्हणून ते पुनर्संचयित करणारे आहेत.
रसायनशास्त्रावरील पाठ्यपुस्तकांमध्ये सापडलेल्या "इलेक्ट्रोनॅगेटीव्हिटी", "ऑक्सिडेशन स्टेट", "रेडॉक्स रिएक्शन" या संकल्पनांची व्याख्या देऊया.
« ऑक्सिडेशन राज्य - कंपाऊंडमधील अणूचा सशर्त शुल्क, त्यामध्ये केवळ आयन असतात असे गृहित धरून गणना केली जाते. ही संकल्पना परिभाषित करताना असे मानले जाते की बाँडिंग (व्हॅलेन्स) इलेक्ट्रॉन अधिक इलेक्ट्रोनॅजेटिव्ह अणूंमध्ये हस्तांतरित केले जातात, आणि म्हणूनच संयुगे सकारात्मक आणि नकारात्मक चार्ज केलेल्या आयनसारखे असतात. ऑक्सिडेशन अवस्था शून्य, नकारात्मक किंवा सकारात्मक असू शकते, जी सहसा शीर्षस्थानी घटक चिन्हाच्या वर ठेवली जाते.
ऑक्सिडेशन अवस्थेचे शून्य मूल्य त्या मुक्त अवस्थेत असलेल्या घटकांच्या अणूंचे श्रेय दिले जाते ... ऑक्सिडेशन स्टेटचे नकारात्मक मूल्य त्या अणूंना असते ज्याकडे बाँडिंग इलेक्ट्रॉन क्लाऊड (इलेक्ट्रॉन जोडी) विस्थापित होते. त्याच्या सर्व संयुगांमध्ये फ्लोरिनसाठी ते -1 आहे. इतर अणूंमध्ये व्हॅलेन्स इलेक्ट्रॉन दान करणा At्या अणूंची सकारात्मक ऑक्सीकरण स्थिती असते. उदाहरणार्थ, अल्कली आणि क्षारीय पृथ्वीच्या धातूंसाठी अनुक्रमे +1 आणि +2 आहे. साध्या आयनमध्ये ते आयनच्या शुल्काइतके असते. बहुतेक संयुगांमध्ये हायड्रोजन अणूंचे ऑक्सिडेशन स्टेट +१ असते, परंतु मेटल हायड्रिड्स (हायड्रोजनसह त्यांचे संयुगे) आणि इतरांमध्ये ते १ -१ असते. ऑक्सिजनसाठी ऑक्सिडेशन अवस्था -2 आहे, परंतु, उदाहरणार्थ, फ्लोरिनच्या संयोजनात ते +2 असेल, आणि पेरोक्साईड संयुगे -1 मध्ये. ...
कंपाऊंडमधील अणूंच्या ऑक्सिडेशन स्टेट्सची बीजगणित बेरीज शून्य असते आणि जटिल आयनमध्ये आयनचा आकार असतो. ...
सर्वाधिक ऑक्सिडेशन स्टेट हे त्याचे उच्च सकारात्मक मूल्य आहे. बहुतेक घटकांसाठी, हे नियतकालिक प्रणालीतील समूहाच्या संख्येइतके असते आणि त्यातील घटकांचे घटकांचे महत्त्वपूर्ण परिमाणात्मक वैशिष्ट्य असते. त्याच्या संयुगात उद्भवणार्\u200dया घटकाच्या ऑक्सिडेशन स्टेटचे सर्वात लहान मूल्य सामान्यत: सर्वात कमी ऑक्सिडेशन स्टेट असे म्हणतात; बाकीचे सर्व मध्यवर्ती आहेत ”(एनसाइक्लोपेडिक डिक्शनरी ऑफ यंग केमिस्ट, लेख“ ऑक्सीकरण स्टेट ”).
या संकल्पनेसंबंधी मूलभूत माहिती येथे दिली आहे. हे दुसर्या संज्ञेशी संबंधित आहे, इलेक्ट्रोनेगेटिव्हिटी.
« विद्युतप्रवाहता - रासायनिक बंधनाच्या निर्मितीत सामील असलेल्या इलेक्ट्रॉनांना आकर्षित करण्यासाठी रेणूमधील अणूची ही क्षमता आहे ”(एन्साक्लोपीडिक डिक्शनरी ऑफ यंग केमिस्ट, लेख“ इलेक्ट्रोनेगेटीव्हिटी ”).
“रेडॉक्सच्या प्रतिक्रियेसह परमाणुंच्या ऑक्सिडेशन अवस्थेमध्ये बदल होतो, ज्यामुळे अणुभट्टी तयार होते, अभिकर्मकांपैकी एकाच्या अणूपासून इलेक्ट्रॉन कमी करणे (एजंट कमी करणे) दुसर्\u200dयाच्या अणूकडे जाते. ऑक्सिडेशन-रिडक्शनची प्रतिक्रिया एकाच वेळी ऑक्सिडेशन (इलेक्ट्रोनचे प्रकाशन) आणि घट (इलेक्ट्रॉनची जोड) उद्भवते "(केमिकल ज्ञानकोश शब्दकोष, एड. आयएल नुनियंट्स, लेख" रेडॉक्स रिएक्शन ").
आमच्या मते, या तीन संकल्पनांमध्ये बर्\u200dयाच चुका लपविल्या आहेत.
प्रथम , आमचा विश्वास आहे की दोन घटकांमधील रासायनिक बंधन तयार करणे हे त्यांचे इलेक्ट्रॉन समाजीकरणाच्या सर्व प्रक्रियेवर नाही. रासायनिक बंध एक गुरुत्व बंधन आहे. न्यूक्लियसभोवती उड्डाण करणारे इलेक्ट्रॉन हे घटकांच्या शरीरात आणि त्या दरम्यानच्या मध्यभागी असलेल्या न्यूक्लियन्सच्या पृष्ठभागावर जमा होणारे विनामूल्य फोटॉन आहेत. दोन घटकांमधील संबंध निर्माण होण्याकरिता, त्यांच्या विनामूल्य फोटोंना घटकांमधे चालण्याची आवश्यकता नाही. हे घडत नाही. वास्तविकतेत, जड घटक फिकट व्यक्तींमधून विनामूल्य फोटॉन काढून टाकतो (आकर्षित करतो) आणि त्यांना (अधिक तंतोतंत, स्वतःच) ठेवतो. आणि फिकट घटकांचा झोन, ज्यामधून हे फोटॉन काढून टाकले गेले होते, कमी-अधिक होते. या झोनमधील आकर्षण काय मोठ्या प्रमाणात प्रकट होते. आणि फिकट घटक जड असलेल्याकडे आकर्षित होते. अशाप्रकारे एक रासायनिक बंध तयार होतो.
दुसरे म्हणजे , आधुनिक रसायनशास्त्र स्वत: कडे विकृत इलेक्ट्रॉनकडे आकर्षित करण्यासाठी घटकांची क्षमता पाहतात - वरची बाजू. असे मानले जाते की एखाद्या घटकाची इलेक्ट्रोनॅक्टिव्हिटी जितकी जास्त असते तितके ते आपल्याकडे इलेक्ट्रॉन आकर्षित करण्यास अधिक सक्षम असते. आणि ऑक्सिजनसह फ्लोरिन बहुधा ते सर्वोत्कृष्ट करते - ते इतर लोकांचे इलेक्ट्रॉन आकर्षित करतात. तसेच 6 आणि 7 गटांचे इतर घटक.
खरं तर, हे मत एक भ्रम करण्यापेक्षा काहीच नाही. हे गैरसमज आधारित आहे की गट संख्या जितकी मोठी असेल तितके घटक जास्त. आणि न्यूक्लियसचा सकारात्मक शुल्क जास्त असेल. हे बुलशिट आहे. शास्त्रज्ञ अद्याप त्यांच्या दृष्टीकोनातून “शुल्क” म्हणजे काय हे समजावून सांगायलाही त्रास देत नाहीत. फक्त अंकशास्त्राप्रमाणे त्यांनी सर्व घटकांची क्रमाने गणना केली आणि संख्येनुसार शुल्क आकारले. छान वाढ!
मुलाला हे देखील स्पष्ट आहे की दाट धातूपेक्षा गॅस हलका आहे. रसायनशास्त्रात असे मानले जाते की गॅस स्वत: कडे इलेक्ट्रॉन आकर्षित करण्यास चांगले असतात?
दाट धातू, अर्थातच, ते इलेक्ट्रॉन आकर्षित करण्यास चांगले आहेत.
रासायनिक शास्त्रज्ञ अर्थातच "इलेक्ट्रोनॅक्टिव्हिटी" ही संकल्पना वापरात येऊ शकतात, कारण ती सामान्य आहे. तथापि, त्यांना त्याचा अर्थ अगदी उलट दिशेने बदलावा लागेल.
विद्युतप्रवाहता इलेक्ट्रॉन स्वतःकडे आकर्षित करण्यासाठी रेणूमधील रासायनिक घटकाची क्षमता आहे. आणि, नैसर्गिकरित्या, ही क्षमता धातूंमध्ये नसलेल्या धातूंपेक्षा अधिक चांगली दर्शविली जाते.
रेणूमधील विद्युत खांबाविषयी, तर खरंच नकारात्मक ध्रुव - हे आकर्षण खालच्या फील्डसह इलेक्ट्रॉन देणगी देणारे नसलेले धातूचे घटक आहेत. ए सकारात्मक - हे नेहमीच मोठ्या प्रमाणात आकर्षण असणारी धातूंचे गुणधर्म असलेले घटक असतात.
चला एकत्र हसू.
विद्युतप्रवाहता - विद्यमान वस्तुमान आणि शुल्कासह रासायनिक घटकाच्या गुणवत्तेचे वर्णन करण्याचा हा आणखी एक प्रयत्न आहे. जसे की बहुतेकदा असेच आहे, विज्ञानाच्या दुसर्या क्षेत्रातील शास्त्रज्ञ, या प्रकरणात, रसायनशास्त्र, जसे की त्यांच्या सहकारी भौतिकशास्त्रज्ञांवर विश्वास ठेवत नाहीत तर ते फक्त कारण की कोणतीही व्यक्ती, शोध लावते, स्वत: च्या मार्गाने जाते आणि फक्त इतरांच्या अनुभवाचा शोध घेत नाही.
यावेळीही ते घडले.
परमाणुंमध्ये परस्परांशी संवाद साधतांना काय घडते हे समजण्यास रसायनशास्त्रज्ञांना वस्तुमान आणि शुल्काने काहीही केले नाही - आणि इलेक्ट्रोनॅगेटीव्हिटीची ओळख झाली - रासायनिक बंधन तयार होण्यामध्ये गुंतलेल्या इलेक्ट्रॉनांना आकर्षित करण्याची घटकांची क्षमता. हे कबूल केले पाहिजे की या संकल्पनेची कल्पना अगदी योग्यरित्या दिली आहे. केवळ त्या दुरुस्तीमुळे ती वास्तविकता प्रतिबिंबित करते. आम्ही आधीच म्हटल्याप्रमाणे, पृष्ठभागाच्या न्यूक्लियन्सच्या रंगाच्या विचित्रतेमुळे - धातूंकडे नव्हे तर धातूंवरही इलेक्ट्रॉन आकर्षित करणे चांगले आहे. धातू हे सर्वात कमी करणारे एजंट आहेत. नॉन-मेटल ऑक्सिडायझिंग घटक आहेत. धातू काढून टाकल्या जातात, धातू नसतात. धातू - यिन, धातू नसलेले - यांग.
निसर्गाची रहस्ये समजून घेण्याच्या बाबतीत विज्ञानात साहाय्य येते.
संबंधित ऑक्सीकरण स्थिती , मग रासायनिक कंपाऊंड - एक रेणूमध्ये विनामूल्य इलेक्ट्रॉनचे वितरण कसे होते हे समजून घेण्याचा हा चांगला प्रयत्न आहे.
जर एक रासायनिक कंपाऊंड एकसंध असेल - म्हणजे ते सोपे आहे, त्याच्या संरचनेमध्ये समान प्रकारच्या घटकांचा समावेश आहे - तर सर्व काही बरोबर आहे, खरंच, कंपाऊंडमधील कोणत्याही घटकाची ऑक्सिडेशन अवस्था शून्य आहे. या कंपाऊंडमध्ये ऑक्सिडायझिंग एजंट नसल्याने आणि कोणतेही कमी करणारे एजंट नाहीत. आणि सर्व घटक समान गुणवत्तेचे आहेत. कोणीही इलेक्ट्रॉन काढून घेत नाही, कोणीही ते देत नाही. तो घन पदार्थ, किंवा द्रव किंवा गॅस असो, काही फरक पडत नाही.
ऑक्सिडेशन स्टेट, इलेक्ट्रोनॅगेटीव्हिटी सारख्या, एका रासायनिक घटकाची गुणवत्ता दर्शवते - केवळ एक रासायनिक घटकाच्या चौकटीत. कंपाऊंडमधील रासायनिक घटकांच्या गुणवत्तेची तुलना करण्यासाठी ऑक्सिडेशन स्टेटची रचना केली गेली आहे. आमच्या मते, कल्पना चांगली आहे, परंतु त्याची अंमलबजावणी पूर्णपणे समाधानकारक नाही.
आम्ही रासायनिक घटकांच्या संरचनेच्या आणि त्या दरम्यानच्या बंधनांच्या संपूर्ण सिद्धांत आणि संकल्पनेच्या विरोधात आहोत. बरं, जर फक्त आमच्या कल्पनांनुसार गटांची संख्या 8 पेक्षा जास्त असली तर याचा अर्थ असा आहे की संपूर्ण यंत्रणा कोलमडत आहे. आणि फक्त तेच नाही. सर्वसाधारणपणे, "एकीकडे" अणूमध्ये इलेक्ट्रॉनची संख्या मोजणे हे कसलेही गंभीर नाही.
सध्याच्या संकल्पनेनुसार, हे दिसून आले की सर्वात लहान पारंपारिक शुल्क सर्वात मजबूत ऑक्सिडंट्सवर नियुक्त केले जाते - फ्लोरिनचा आकार सर्व संयुगांमध्ये -1 असतो, जवळजवळ सर्वत्र ऑक्सिजन -2 असतो. आणि अत्यंत सक्रिय धातूंसाठी - अल्कधर्मी आणि क्षारीय पृथ्वी - हे शुल्क अनुक्रमे +1 आणि +2. हे मुळीच तार्किक नाही. जरी, आम्ही पुन्हा सांगत आहोत, ही सर्वसाधारण योजना ज्याच्या अनुषंगाने केली गेली आहे हे आम्हाला चांगले समजले आहे - सर्व टेबलमधील 8 गट आणि बाह्य उर्जा पातळीवरील 8 इलेक्ट्रॉन यांच्या फायद्यासाठी.
कमीतकमी, हॅलोजन आणि ऑक्सिजनच्या शुल्काचे मूल्य वजा चिन्हासह सर्वात मोठे असावे. आणि क्षार आणि क्षारीय पृथ्वीच्या धातूंमध्ये हे देखील मोठे आहे, केवळ एका अधिक चिन्हासह.
कुठल्याही रासायनिक कंपाऊंड असे घटक आहेत जे इलेक्ट्रॉन देतात - ऑक्सिडायझर्स, नॉन-मेटल, नकारात्मक शुल्क आणि इलेक्ट्रॉन दान करणारे घटक - एजंट्स, धातू, सकारात्मक शुल्क कमी करतात. अशा प्रकारे घटकांची तुलना करणे, त्यांचा एकमेकांशी संबंध जोडणे आणि त्यांची ऑक्सीकरण स्थिती निश्चित करण्याचा प्रयत्न करणे हे आहे.
तथापि, अशा प्रकारे शोधण्यासाठी ऑक्सिडेशन स्थिती, आमच्या मते, वास्तवात अगदी अचूकपणे प्रतिबिंबित होत नाही. रेणूमधील घटकांच्या इलेक्ट्रोनेगेटिव्हिटीची तुलना करणे अधिक योग्य ठरेल. तथापि, इलेक्ट्रोनेगेटिव्हिटी ऑक्सिडेशन स्टेटसारखेच आहे (केवळ एका घटकाची गुणवत्ता दर्शवते).
आपण इलेक्ट्रोनॅगेटीव्हिटीचा स्केल घेऊ शकता आणि प्रत्येक घटकाच्या सूत्रात त्याची मूल्ये लिहू शकता. आणि मग हे तत्काळ दिसून येईल की कोणते घटक इलेक्ट्रॉन सोडतात आणि कोणते काढून टाकतात. कंपाऊंडमध्ये ज्याची इलेक्ट्रोनॅक्टिव्हिटी सर्वात मोठी आहे - नकारात्मक ध्रुव, इलेक्ट्रॉन देतात. आणि ज्याची विद्युतक्षमता सर्वात लहान आहे - सकारात्मक ध्रुव, इलेक्ट्रॉन घेते.
रेणूमध्ये 3 किंवा 4 घटक असल्यास, काहीही बदलत नाही. आम्ही इलेक्ट्रोनॅगेटीव्हिटीची व्हॅल्यूज देखील ठेवतो आणि तुलना करतो.
तथापि, आपण रेणूच्या संरचनेचे मॉडेल काढण्यास विसरू नका. खरंच, कोणत्याही कंपाऊंडमध्ये, ते सोपे नसल्यास, म्हणजेच, त्यात एक प्रकारचा घटक नसतो, सर्वप्रथम धातु आणि धातू नसलेल्या एकमेकांशी जोडलेले असतात. धातू नॉन-मेटलमधून इलेक्ट्रॉन घेतात आणि त्यांना बांधतात. आणि धातू नसलेल्या एका घटकातून इलेक्ट्रॉन अधिक एकाच वेळी 2 किंवा त्याहून अधिक घटकांकडून अधिक स्पष्ट धातूंच्या गुणधर्मांद्वारे घेतले जाऊ शकतात. अशाप्रकारे एक जटिल, जटिल रेणू उद्भवते. परंतु याचा अर्थ असा नाही की अशा रेणूमध्ये धातूचे घटक एकमेकांशी मजबूत बंधनात प्रवेश करतात. कदाचित ते एकमेकांच्या विरुद्ध बाजूवर असतील. पुढील असल्यास ते आकर्षित होतील. परंतु एका घटकामध्ये इतर घटकांपेक्षा जास्त धातूचा संबंध असल्यासच एक मजबूत बंध तयार होतो. एक घटक इलेक्ट्रॉन निवडणे अत्यावश्यक आहे - त्यांना काढून टाकते. अन्यथा, घटक उघड होणार नाही - पृष्ठभागावरील विनामूल्य फोटोंमधून मुक्ति. आकर्षण फील्ड स्वतःच प्रकट होणार नाही आणि कोणतेही मजबूत कनेक्शन होणार नाही. तो गुंतागुंतीचा विषय - शिक्षण रासायनिक बंध, आणि आम्ही या लेखात याबद्दल तपशीलवार जाणार नाही.
आमचा विश्वास आहे की आम्ही "इलेक्ट्रोनेगेटिव्हिटी", "ऑक्सिडेशन स्टेट", "ऑक्सिडेशन" आणि "रिडक्शन" या संकल्पनेच्या विश्लेषणासाठी समर्पित विषय विस्तृतपणे कव्हर केला आहे आणि आपल्याला बरीच मनोरंजक माहिती प्रदान केली आहे.
मार्गदर्शित स्वप्नांच्या पुस्तकातून लेखक मीर एलेनाजीर्णोद्धार “जेव्हा वैयक्तिकृत करण्याचे एकल चिन्ह जन्माला येते तेव्हा सार आणि जीवन दोन भागात विभागले जाते. आतापासून, जोपर्यंत अंतिम शांती होत नाही तोपर्यंत सार आणि जीवन पुन्हा कधीही एकमेकांना दिसणार नाही. " विल्यम, कॉलेज नंतर "द गोल्डन फ्लॉवरचा गुपित"
सिक्रेट्स ’या पुस्तकातून. पृथ्वीवर आणि पलीकडे अविश्वसनीय स्पष्ट लेखक व्याटकिन अर्काडी दिमित्रीविचस्वैच्छिक व्हँपायरिझमची अत्यधिक पदवी म्हणून मास्कोच्म या अर्थाने, मास्चॉझिझम कोडेंडेंडन्सीसारखेच आहे. मास्कोसिस्ट असे लोक आहेत ज्यांना स्वतःच्या शारीरिक आणि मानसिक दुःखातून आनंद मिळतो. दुस words्या शब्दांत, त्यांना मारहाण करणे, फटकारणे, गुंडगिरी करणे आवडते
रशिया मधील व्हँपायर्स या पुस्तकातून. आपल्याला त्यांच्याबद्दल माहित असणे आवश्यक असलेली प्रत्येक गोष्ट! लेखक बाऊर अलेक्झांडररक्ताच्या तोटाचे स्तर कसे ठरवायचे जेव्हा व्हॅम्पायर रक्त पितो, तो एकावेळी अर्धा लिटर ते दीड लिटर रक्त पितो. मानवी शरीरात केवळ पाच ते सहा लिटर रक्त असते, म्हणून अशा रक्त कमी होणे जीवघेणा नसते. तथापि, एक पिशाच करू शकता
मॉडेलिंग द फ्यूचर इन अ ड्रीम या पुस्तकातून लेखक मीर एलेनापुनर्प्राप्ती पदवीनंतर, एक बंद एंटरप्राइझमध्ये अभियंता म्हणून काम करताना मला समजले की मी माझ्या जागी नाही, म्हणून मी माझा व्यवसाय बदलण्याचे ठरविले आणि जाझ स्कूल ऑफ इम्प्रूव्हिझेशन, आणि नंतर संगीत शाळेच्या शास्त्रीय विभागात प्रवेश केला.
फेंग शुई या गोल्डन रुल्स या पुस्तकातून. यश, कल्याण आणि दीर्घायुसाठी 10 सोप्या चरण लेखक ओगुडिन व्हॅलेंटीन लिओनिडोविचबाह्य वस्तूंच्या नकारात्मक प्रभावाची पदवी बाह्य वस्तूंवर थेट घराच्या प्रवेशद्वारासमोर असल्याने सर्वात मोठा नकारात्मक प्रभाव पडतो. परंतु जितके अधिक ते प्रवेशद्वाराच्या कोनात स्थित आहेत तितके त्यांचे प्रभाव कमकुवत होते.
लेखक शुरे एडवर्डपहिली पदवी: पाककला. डोंगरावरील प्रवचन आणि देवाचे राज्य ख्रिस्ताच्या कार्याची सुरुवात गॅलील लोकांची सुवार्ता आणि "देवाचे राज्य" या घोषणेने होते. ही भविष्यवाणी आपल्याला त्याच्या लोकप्रिय शिकवणांकडे सूचित करते. त्याच वेळी, ही अधिक उदात्त होण्याची तयारी आहे
दैवी उत्क्रांति या पुस्तकातून. स्फिंक्सपासून ख्रिस्तापर्यंत लेखक शुरे एडवर्डदीक्षा (शुद्धिकरण) ची दुसरी पदवी. चमत्कारी उपचार ख्रिश्चन थेरपी सर्व प्राचीन रहस्यांमध्ये, नैतिक आणि बौद्धिक तयारी नंतर आत्म्याच्या शुध्दीकरणाद्वारे होते, ज्याने त्यामध्ये नवीन अवयव पुनरुज्जीवित केले पाहिजे आणि नंतर त्यास क्षमता दिली पाहिजे
दि रिझल ऑफ द ग्रेट स्फिंक्स या पुस्तकातून लेखक बार्बरेन जॉर्जसपुतळ्याची जीर्णोद्धार ग्रेट स्फिंक्सचे वास्तविक वय अ\u200dॅडमिक युगच्या सुरुवातीस आहे. अगदी थोडक्यात, तो पिरॅमिडचा समकालीन आहे, ज्याचे त्यांनी आपल्या आधीचे वर्णन केलेले वर्णन स्वतःच पूर्ण केले आहे. गेल्या शतकानुशतके ग्रेट स्फिंक्सची प्रतिमा उघडकीस आली आहे.
हीलिंग द सोल या पुस्तकातून. 100 चिंतन तंत्र, उपचारांचे व्यायाम आणि विश्रांती लेखक रजनीश भगवान श्रीताल पुनर्संचयित करा ... झोपायला त्याच वेळी सेट करा - दररोज संध्याकाळी अकरा असल्यास, नंतर अकरा हे पहिले आहे: विशिष्ट वेळेस प्रारंभ करा आणि लवकरच शरीर या लयमध्ये प्रवेश करण्यास सक्षम असेल. यावेळी बदलू नका, अन्यथा आपण शरीराला गोंधळ घालता. शरीर
लेखक कुज्मिशिन ई.एल.Rentप्रेंटिस डिग्री Appप्रेंटिस पदवी प्रवेश बॉक्स आणि वेस्टमेंट्सची सजावट बॉक्सच्या भिंती आणि कमाल मर्यादा नीलिंगीशिवाय निळ्या आणि पांढ white्या कपड्याने टांगल्या पाहिजेत. उपासनाशील मास्टरच्या मस्तकाच्या वरच्या दिशेने मध्यभागी लिहिलेले एक त्रिकोण त्रिभुज आहे
कॅग्लिओस्ट्रो आणि इजिप्शियन फ्रीमासनरी यांच्या पुस्तकातून लेखक कुज्मिशिन ई.एल.लॉज आणि व्हेस्टमेंट्सच्या Appप्रेंटिस सजावटीच्या पदवीसाठी प्रवेश लॉजच्या भिंती आणि कमाल मर्यादा नीलिंगी आणि पांढर्\u200dया कपड्याने टांगल्या पाहिजेत. व्हेनेरेबल मास्टरच्या मस्तकाच्या वरच्या दिशेने तेजोभोवती त्रिकोण आहे ज्याच्या मध्यभागी "यहोवा" नावाने लिहिलेले आहे, भरतकाम केलेले
‘आत्मकथा’ या योगी या पुस्तकातून लेखक योगानंद परमहंसधडा 23 मी विद्यापीठाची पदवी मिळवत आहे - आपण आपल्या पाठ्यपुस्तकाच्या तात्विक परिभाषांकडे दुर्लक्ष कराल, परीक्षेत मार्गदर्शन करण्यासाठी काही विवादास्पद "अंतर्ज्ञान" मोजत नाही यात शंका नाही. परंतु आपण त्वरेने एखाद्या अधिक वैज्ञानिक पद्धतीकडे वळत नसाल तर मला करावे लागेल
कबालाच्या पुस्तकातून. उच्च जग. मार्गाची सुरुवात लेखक लेटमन मायकेल7.5. “तोराह देणे” या लेखात स्पष्ट केले आहे की वाईटपणाची प्राप्ती आणि आनंद हा गुणधर्मांमधील निर्मात्याशी समानता दर्शविण्याद्वारे केला जातो, परंतु दु: ख आणि अधीरता निर्माणकर्त्याच्या फरकानुसार ठरविली जाते. त्यानुसार स्वार्थ आपल्यासाठी घृणास्पद आणि असह्य वेदनादायक आहे,
पर्याय 1
1. खालील संयुगांमध्ये रासायनिक घटकांच्या अणूंच्या ऑक्सिडेशन स्थितीचे निर्धारण कराः एचएनओओ, एनओए, एचएनएन, एसओ, एनओओ.
२. नियतकालिक सारणीचा वापर करून, घटत्या विद्युतप्रक्रियेच्या क्रमाने खालील घटकांची व्यवस्था करा: ओ, एन, बी, बी, ली, सी फ्लोरिन व सोडियम या ओळीत कोठे असावेत हे ठरवा. उत्तर समजावून सांगा. 
S. एसओ₂ ते एसओ₃ च्या ऑक्सीकरण दरम्यान सल्फर अणूच्या ऑक्सिडेशनची स्थिती कशी बदलते? उत्तर समजावून सांगा.
पर्याय 2
1. खालील संयुगांमध्ये रासायनिक घटकांच्या अणूंच्या ऑक्सिडेशन स्थितीचे निर्धारण करा: सीओई, एचपीओ, सिह, पोओ, एमजीसी.
२. कोणत्या रासायनिक घटकाच्या अणूच्या दिशेने सामान्य इलेक्ट्रॉनिक जोड्या, खालील संयुगेच्या रेणूंमध्ये: बीएफ₃, पीसीएलई, सीएस₂, सीसीएल₄, एचबीआर? एक तर्कसंगत उत्तर द्या.
3. निर्मिती दरम्यान कार्बनची ऑक्सीकरण स्थिती बदलते काय? कार्बनिक acidसिड कार्बन डाय ऑक्साईड आणि पाणी पासून H₂CO₃? उत्तर समजावून सांगा.
पर्याय 3
1. खालील संयुगांमध्ये रासायनिक घटकांच्या अणूंच्या ऑक्सिडेशन स्थितीचे निर्धारण करा: क्ले, नाकलो, कॅक्ली, एचएफ, एसओ, क्लोओ.
2. वापरणे नियतकालिक प्रणाली रासायनिक घटक, त्यांच्या विद्युतप्रवाहतेच्या चढत्या क्रमाने खालील घटकांची व्यवस्था करतात: पी, अल, क्ल, ना, एस, एमजी. पोटॅशियम आणि फ्लोराईडसाठी या ओळीत एक जागा शोधा. उत्तर समजावून सांगा. 
Met. कार्बन मोनोऑक्साइड (चतुर्थ) आणि पाण्याच्या निर्मितीसह मिथेन सीएच comb च्या ज्वलनवर कार्बनची ऑक्सिडेशन स्थिती कशी बदलते? उत्तर समजावून सांगा.
पर्याय 4
1. खालील संयुगांमध्ये रासायनिक घटकांच्या अणूंच्या ऑक्सिडेशन स्थितीचे निर्धारण करा: H₂SO₄, SO₂, NO₂, BF₃, H₂S.
२. काय च्या अणू दिशेने रासायनिक घटक खालील संयुगेच्या रेणूंमध्ये सामान्य इलेक्ट्रॉन जोड्या विस्थापित होतात: H₂O, PCl₃, H₃N, H₂S, CO₂? एक तर्कसंगत उत्तर द्या.
Water. जेव्हा पाणी तयार होते तेव्हा अणूंचे ऑक्सीकरण स्थिती बदलू नका? साधे पदार्थ - हायड्रोजन आणि ऑक्सिजन? उत्तर समजावून सांगा.


