Цахилгаан эрчим хүч нь химийн электроныг агууламжаар агууламжийн атомыг агуулсан бусад электронуудтай холбосон электронуудтай холболтын атомыг агуулдаг.
Химийн бонд нь өөр өөр элементийн хооронд үүсэх үед ерөнхий цахим үүл нь цахим цахим үүлний хоорондох цахим үүл, мөн цанат, электрономенгатын өөрчлөлттэй байдаг.
Химийн томъёо бичихдээ цахилгаан эрчим хүчийг харгалзан үзэх болно: Хамгийн их цахилгаан холбооны элемент нь хоёртын холболтонд тэмдэглэгддэг.
Цахилгаан эрчим хүч нь үе мөч бүрийн элементүүдийг баруун тийш чиглүүлж, нэгээс доошоо чиглүүлж, ижил PS бүлгийн элементүүдээс доошоо чиглүүлнэ.
Аөцаа Элемент нь түүний атомын өмчийг бусад олон тооны атомтай холбодог.
StoIchiometric, цахим валент ба зохицуулалтын дугаар байдаг. Бид зөвхөн StoIchiometric Valence-ийг авч үзэх болно.
StoIchiometrice Валенци нь өөр элемент хэдэн атомыг харуулж байгааг харуулж байна. Учир нь устөрөгчийн нэгжийг устөрөгчийн эзэлсэн валентен батлагдсан тул Устөрөгч нь үргэлж Моновентент байдаг. Жишээлбэл, HCL, H 2 O, NH 3 нийлбэр нь (аммогин H 3 n-ийг (аммиакен, хүчилтөрөгчийн трамент, Нотроцений тривен, Нотроцений тривен, Нотроцений тривен, Нотроцений тривен, Нотроцений тривен, Нотроцений тривен, нүүрстөрөгчийн тривенци, Нотроцений тривен, нүүрстөрөгчийн тривен, Нотроцений тривен, нүүрстөрөгчийн тривен, нүүрстөрөгчийн тривен, Нотроцен, НИРОГЕНЕРЕНЕРИЕНЕР, НОГООНЫ ТУХАЙ, НИРООГЕНЕРИЙН ХУВЬЦАА.
Оксиометрийн үнэт эдлэл нь ихэвчлэн 2. бараг бүх элементүүд хүчилтөрөгчтэй нийлдэг бөгөөд энэ нь хүчилтөрөгчтэй нэгдлүүдийг үүсгэдэг. Энэ нь өөр элементийн валентыг тодорхойлоход тохиромжтой. Жишээлбэл, На 2 О, Ко, 2 O 2 O, SO 2 O3, SO 3 натри Моновент, Траваторын моновентент, кобальт моновентент, кобальт Монивент, Тривалент, Төрөгч нь Траваторын монитент, кобальт Мөр 3 нь Траваторын моновентент, Төрөгчийн тривент, Төрөгчийн тривент, Төрөгчийн травентент, Тривалент, Төрөгч нь Сулальт Монивент, Тривалент, Төрөгчийн тривент, хүхрийн цамц юм.
Исэлдүүлэгч, нөхөн сэргээх урвалд оролцох нь бидний хувьд иземийн бүсийн зэрэгийг тодорхойлох нь чухал байх болно.
Исэлдэлтийн зэрэг Бодис дахь элемент нь StoIchiomettric Valence-ийг Plus тэмдэг эсвэл хасах замаар авсан.
Химийн элементүүдийг элемент болгон хуваана байнгын валенц Валентийн хувьсах элементүүд.
1.3.3. Молекул ба уян хатан бодис. Болор торны төрөл. Тэдгээрийн найрлага, бүтцийн шинж чанараас хамаарал нь хамаарал.
Байгаль орчинд аль мужид байхаас хамаарна, тэдгээрийг молекул ба эерэг бус байдлаар хуваана. -Аар / -оор молекулын бодис Хамгийн жижиг бүтцийн тоосонцор нь молекулууд юм. Эдгээр бодис нь молекулын болор тортой. Мөрөөдлийн бус бодис, атом эсвэл ион нь хамгийн жижиг бүтцийн тоосонцор юм. Болор тор нь атомын, ион эсвэл металл юм.
Болор торны төрөл нь бодисын шинж чанарыг ихэвчлэн тодорхойлдог. Жишээлбэл, металлууд болор торны төмөр хэлбэрбусад бүх элементүүдээс ялгаатай Өндөр хуванцар, цахилгаан ба дулааны дамжуулалтБайна уу. Эдгээр шинж чанарууд, түүнчлэн бусад хүмүүсийн болон бусад олон хүмүүс - хуурамч, металл гялалзах гэх мэт. металлын атомын хоорондох харилцааны тусгай хэлбэрээс болж металл холболт. Металлуудын өвөрмөц шинж чанар нь зөвхөн конденсатор мужид илэрдэг гэдгийг тэмдэглэх нь зүйтэй. Жишээлбэл, Мөнгө нь Gasous мужид металлын физик шинж чанартай байдаггүй.
Металлын тусгай төрлийн харилцаа холбооны тусгай хэлбэр нь металл юм - валентийн электронуудын дутагдалтай тул тэд металлын бүх бүтцэд хамаарна. Металлын бүтцийн хамгийн энгийн загвар нь Fressalley LATALE нь электронууд, электронуудаар хүрээлэгдсэн эерэг, электронуудын хөдөлгөөнүүдээс бүрдсэн эерэг, электронууд, хийн молекулууд шиг эмх замбараагүй байдал үүсдэг гэж үздэг. Гэсэн хэдий ч ийм загвар, металлын олон шинж чанар, тоон шалгалтанд тэнцвэртэй тайлбар өгөх нь хангалтгүй юм. Металлын улсын онолыг хөгжүүлэх нь бүтээлийг бүтээсэн металын онолын онолнь квант механикийн тоглолт дээр үндэслэсэн болно.
Болор торны зангилаанд нь категор, металл атомууд байдаг бөгөөд элбэнд, электронууд нь болор торны дагуу чөлөөтэй хөдөлдөг.
Металлын онцлог шинж чанар нь уян налирхай чанарТэдний талстуудын дотоод бүтцийн өвөрмөц байдлаас болж. Ид шидийн дор, гадны нөлөөг арилгахын тулд гадны хүчний дагуу бие махбодийн идэвхиний чадварын дагуу бие махбодийн чадварын дагуу бие махбодийн чадварын дагуу. Металлын энэ өмч нь тэдэнд огтлох үед тэдэнд огтлоход өөр хэлбэрийг өгөхөд хүргэдэг, эсвэл металлаар явах, эсвэл утсыг утсан руу татах боломжийг олгодог.
Металлын хуванцар нь болор латтисыг үүсгэдэг, бие биетэйгээ харьцуулахад харьцангуй өөрчлөгдөж, бие биентэйгээ харьцуулахад харьцангуй өөрчлөгддөг. Энэ нь EON-ийн давхрын улмаас электроныг нүүлгэж байгаа тул электронуудыг нүүлгэн шилжүүлэх үр дүнд ION давхаргын хооронд харилцаж байна. Цөмийн үр нөлөөг цөмийн гриллээр бэхэлсэн бөгөөд түүний тусдаа давхаргууд шилжсэн бөгөөд тэдгээрийн хоорондох наалдамхай нь салалтаас болж эвдэрсэн байна ковусент хэлэв.
ионуудДараа нь эдгээр бодисууд хэлбэр ион бол болор торны төрөл.

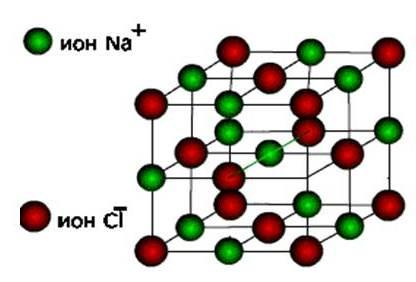
Эдгээр нь давс, түүнчлэн ердийн металлын исэл, гидроксид юм. Эдгээр нь хатуу, эмзэг бодисууд, гэхдээ тэдний үндсэн чанар : Эдгээр нэгдлийн уусмал, хайлмал нь цахилгаан гүйдэлтэй.
Хэрэв болор торны зангилаанд байрладаг бол атомалДараа нь эдгээр бодисууд хэлбэр атомын төрөл нь болор торны төрөл(Алмазан, Бороо, Силикон хөнгөн цагаан, цахиурын исэл). Проперти, маш хатуу, хатуу, хугарал, усанд уусдаг.
Хэрэв болор торны зангилаанд байрладаг бол молекулуудЭдгээр бодисууд хэлбэр (хий, шингэний хэвийн нөхцөлд: o 2, hcl; i 2 органик бодисууд).
30 o C.-ийн температурт хайлж, 30 o C. Энэ аномалиаг, энэ аномали нь GA 2 молекул ба түүний шинж чанарууд нь бодистой төстэй байх болно молекулын талст гриллтэй байх.
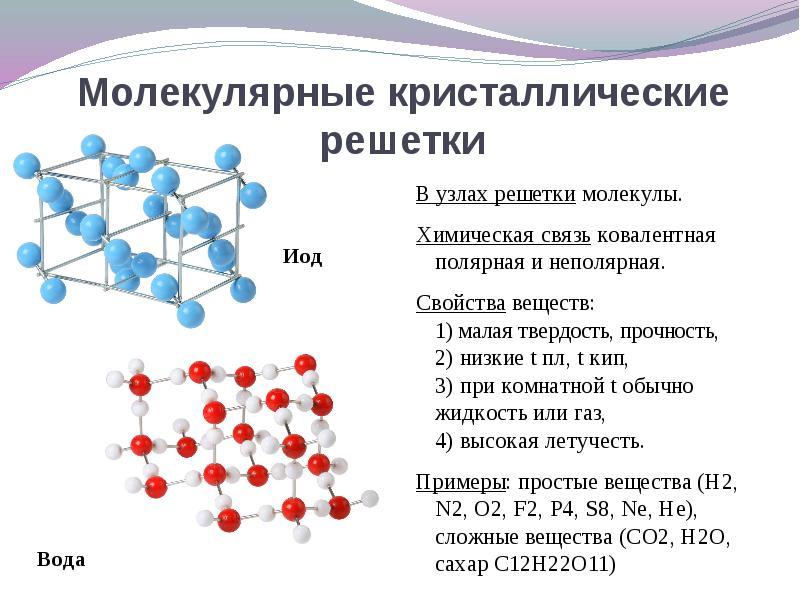
Жишээ.Немолекулын бүтэц нь бүлгийн бүх металлуудтай байдаг.
1) нүүрстөрөгч, Борон, Силикон; 2) фтор, бром, иод;
3) хүчилтөрөгч, хүхэр, азот; 4) хлор, фосфор, Селени.
-Аар / -оор уян хатан бодис Хамгийн жижиг бүтцийн тоосонцор нь атом эсвэл ион юм. Болор тор нь атомын, ион, металл юм
Төлөө хариу Энэ асуулт нь эсрэгээс явахад илүү хялбар байдаг. Хэрэв болор торны зангилаанд байрладаг бол молекулуудДараа нь эдгээр бодисууд хэлбэр молекулын төрөл(Хий, шингэний хэвийн нөхцөлд: o 2, hcl; i 2, rcls sulfur s 8, цагаан фосфур s 4, цагаан фосфурын P 4, органик бодис). Шинж чанараараа эдгээр нь эмзэг бага хайлж буй нэгдэл юм.
Хоёрдахь хариултанд флюрин хий байдаг, гуравдугаарт - хийн хүчилтөрөгч, азот, азот, азот, нитроген. Тиймээс эдгээр бодисууд нь молекулын болор тор, молекулын бүтэцтэй байдаг.
-Аар / -оор хамгийн түрүүнд Бүх бодисын бүх зүйлд хариулж, хэвийн нөхцөлд байгаа хатуу нийлбэрийг хариулж, цөмийн грилл үүсгэдэг бөгөөд ёс зүйгүй гэсэн үг юм.
Зөв хариулт:1) нүүрстөрөгч, Бороо, цахиур
- Хамгийн бага электрон судлал нь химийн элемент юм.
- төмөр
- урлагийн нунтаг
- калөций
Анхаарлыг "хамгийн бага цахим цахилгаан" гэсэн хэллэгт төлөх ёстой. I.E. Хамгийн том төмөр шинж чанартай элемент. Энэ аргумент нь боломжит AZOT хариултыг Metall биш, кальцийн хамгийн идэвхтэй, кальцийн хамгийн идэвхтэй байх ёстой. Хариулт: 4.
- Молекулуудын аль нэг дэх хамгийн туйлын химийн бонд
- CL 4.
- Гэгээн 4.
Электрон систем дэх өөрчлөлтийн хэв маягийн талаархи өөрчлөлтийн талаархи мэдээллийн хэв маягийг давталтын үе шатны үйрмэгийн квадратын квадратын жагсаалтаас хасах нь CF 4-ийг CF 4 дээрээс хасах боломжтой Бүх химийн элементүүдийн хамгийн их цахилгаан тэжээл бүхий нүүрстөрөгчийн нэгдэл - флюрин. Хариулт: 2
- Хлорид молекул, хлорений химийн харилцаа холбоо, тус тусад нь
- ионик ба ковалентен туйл
- ионик ба ковалент бус туйл
- ковалент ба ковалент ба ковалент бус туйл
- устөрөгч ба ковалент бус туйл
Энэ даалгаврыг хурдан, зөв \u200b\u200bгүйцэтгэлийн түлхүүр үг нь "тус тусад нь" гэсэн үг юм. Санал болгож буй хувилбаруудад зөвхөн хариултуудын нэг нь "ковалентент туйлын" гэсэн үгнээс эхэлдэг. I.E. хлорорын шинж чанаруудаас эхэлдэг. Хариулт: 3.
- Нийлмэл байдлаар манганезийн зэрэг олгох нь нийлбэр, 2 MNO 4-тэй тэнцүү, тэнцүү
Томъёоны элементүүдийн зэрэгийг тооцоолох дүрмийн талаархи мэдлэг нь зөв хариултыг сонгох боломжийг танд олгоно. Хариулт: 3.
- Хамгийн жижиг нь исэлдэлтийн хамгийн бага зэрэг нь давстай үрэвсэлтэй байдаг
- хүхрийн кали
- хүхрийн кали
- хүхрийн хөндийн кали
- кали гидрозультефат
Мэдээжийн хэрэг, энэ даалгаврыг хурдан биелүүлэх нь томъёонд давсны нэрийг томъёолох болно. Сульфур бол бүлгийн элемент нь бүлгийн элемент бөгөөд дараа нь хамгийн бага исэлдэлт юм. Энэ утга нь Formula K 2 S - калийн сульфид бүхий нийлмэл нийлбэртэй тохирч байна. Хариулт: 3.
- Исэлдэлтийн зэрэг нь +5 хлорин атом нь ионтой байдаг
- C1O - 4.
- C1o -
- C1o - 3.
- C1O - 2.
Энэ даалгаврыг биелүүлэхдээ цахим сөрөг зүйл байхгүй, гэхдээ нэг сөрөг хүчинтэй ("- -" - "- -"). Ион иж бүрэн исэлдцийн зэрэг нь ион, ионы цэнэглэлттэй тэнцүү бол eOngy of oxtygen атом нь -6 (+5 - 6 \u003d -1) байх ёстой. Хариулт: 3.
- Исэлдэлтийн зэрэг -3 -3 азотын зэрэг нь хоёр холболт тус бүрт байдаг
- NF 3 ба NH 3
- NH 4 CL ба N 2 O 3
- NH 4 CL ба NH 3
- HNO 2 ба NF 3
Зөв хариуг тодорхойлохын тулд зүүн ба баруун дохиоллын хариултыг сэтгэцийн сонголтыг сэтгэхэд шаардлагатай байдаг. Дараа нь нэгдлүүд нь илүү энгийн найрлагатай байхаа сонгоно уу. Бидний хэрэгт энэ тохиолдолд энэ бол энэ бол зөв хоёртын нэгдэл юм. Шин дүн шинжилгээ нь 2 ба 4-р хариу, oxide-ийн exide, oxide-ийн exidation, oxide and exiore and exidational explonegation элементтэй адил. Энэ аргумент үүнийг хасах боломжтой бөгөөд энэ нь анхны бодис юм. Энэ бол анхны бодис юм. Энэ бүхэн ижил азотын фтор Хариулт: 3.
- Молекулын бүтэц нь ороогүй болно
- нүүрстөрөгчийн давхар исэл
- метан
- хир хаана бүтэх
- кальцийн карбонат
Та сөрөг дүгнэлтэд анхаарлаа хандуулах хэрэгтэй. Даалгаврын нөхцөлд тавьсан. Ердийн нөхцөлд мансууруулах бодисын бодисууд нь хатуу төлөвт молекулын талстууд молекулын гриллтэй байдаг тул хуваарилалтын нөхцөл байдал нь нөхцөл байдалд тохирохгүй байна. Тооцооллын карбонататын хамаарал нь давстай дахин хариултыг баталгаажуулна. Хариулт: 4.
- Бодис ба тэдгээрийн бүтцийн шинж чанаруудын талаархи дараахь дүгнэлтүүд мөн үү?
A. Нойтон дотуур дотуур хувцас нь хяруу үед хүйтэн жавартай хатаана.
B. Усны молекулууд бага зэргийн молекул жинтэй тул хүйтэн нойтон дотуур хувцас хатаана.
- зӨВХӨН ЗӨВХӨН А.
- зөв зөвхөн B.
- хоёулаа хоёулаа үнэн
- хоёулаа хоёулаа худлаа.
Мэдлэг биеийн хөгжлийн шинж чанарууд Молекулын бүтэц нь хяруу үед хуурай угаалгын нунтаг хатаах шалтгаан нь мөсний мөсний бүтэц биш бөгөөд усны молекулын бүтэц биш юм. Хариулт: 1.
- Молекуляр бүтэц нь бүх бодис тус бүрт, мөрөнд өгөгдсөн томъёолол байдаг
- CO 2, HNO 3, SAO
- NA 2 S, BR 2, 2, 2
- H 2 SO 4, CU, CU, O 3
- Тэгэхээр 2, I 2, NSL
Санал болгож буй сонголтууд нь гурван бодис агуулагдсан тул эдгээр хувилбаруудыг гурван босоо дохио болгон хуваах нь логик юм. Тэдгээрийн дүн шинжилгээ хийх, энгийн найрлагаас эхэлж, илүү энгийн найрлагаас (дундаж Podstolbik) -ийг агуулж эхэлнэ. Зөв дохиоллын ижил төстэй дүн шинжилгээ нь 1-р дэлхийн металлын исэл (ионогоос бүрдэнэ) -ийг агуулсан хариуг арилгах боломжтой болно. Үлдсэн хоёр сонголтын хоёр сонголтыг оруулах нь 2-р сонголтыг хасах шаардлагатай бөгөөд энэ нь Alkali Metper Sulpey (ION LANTICE) -ийг агуулдаг. Хариулт: 4.
Бие даасан ажлын даалгавар
- Исэлдэлтийн зэрэг нь +5 азотын үзэсгэлэнт нь нийлмэл үзэсгэлэнт, томъёо, томъёо юм
- N 2 o 5
- N 2 o 4
- N 2 о.
- Нийлмэл хром-ийн исэлдэлтийн зэрэг нь (NH 4) 2 CR 2 O 7, тэнцүү томъёо
- Азотын исэлдэлтийн зэрэг нь of and and and нь бодисын дарааллаар буурдаг
- NH 3, 2, 2, KNO 3
- N 2 o 4, kno 2, nh 4 cl
- N 2, n 2 o, nh 3
- HNO 3, HNO 2, NO 2
- Хлорыг исэлдүүлэх зэрэг нь хэд хэдэн бодисыг нэмэгдүүлдэг, томъёо хэлбэрээр нэмэгддэг
- Nslo, nslo 4, kslo 3
- CL 2, C1 2 O 7, KSLO 3
- Ca (c1o) 2, kslo 3, nslo 4
- Ksl, kslo 3, kslo
- Молекул дахь хамгийн туйлын химийн харилцаа холбоо
- шувтэр
- сероводород.
- бромомодород
- fressoDodovodoD
- Ковалент бус туйлын бус бондтой бодис
- цагаан фосфор
- хөнгөн цагаан фосфид
- фосфор хлорид (v)
- кальцийн фосфат
- Дараалсан INON BOD-тэй холбоотой бодисын томъёо
- натрийн хлорид, фосфор хлорид (v), натрийн фосфат
- нилнэмь, нарбам зууралт, шатахын аимбит хувцас
- sELOBLERER, CACERIE CORBIELE
- кальцийн фтори, кальцийн оксид, кальцийн исэл
- Атомын болор тортой
- нойд исль
- калифийн исөл
- хүхрийн Оксид (IV)
- цайны сөл
- Иониктай холболт болор тор хлорыг харилцах үед үүссэн
- фосфорус
- нумын
- устөрөгч
- саарал
- Дараахь дүгнэлтүүд аммони хлоридын тухай үү?
A. Ammonium хлорид бол ковалент ба ионы ярианы бүтэц юм.
B. Ammone-ийн хлорид - ионы бүтэц, тиймээс хатуу, хугарал, дэгдэмхий бус, дэгдэмхий бус.
- зӨВХӨН ЗӨВХӨН А.
- зөв зөвхөн B.
- хоёулаа хоёулаа үнэн
- хоёулаа буруу байна
08. Цахилгаан, исэлдэлтийн зэрэг, исэлдэлт, исэлдэлт, сэргэлт
Химийн чиглэлээр байдаг маш сонирхолтой ойлголтын утга учрыг ярилцъя, шинжлэх ухаанд хангалттай төөрөлдүүлж, урвуу хэлбэрээр хэрэгжиж, хэрэглэгддэг. Энэ нь "EnlongeAngity", "exidation-ийн зэрэг" ба "exidation" ба "Redox Instess" -ын зэрэгтэй болно.
Энэ юу гэсэн үг вэ - үзэл баримтлал нь урвуу хэлбэрт хэрэглэгддэг үү?
Бид энэ талаар аажмаар хэлэхийг хичээх болно.
Цахилгаан Биднийг химийн элементийн редтокс шинж чанарыг харуулдаг. Энэ бол чөлөөт фотонуудыг авах, өгөх чадвар юм. Мөн энэ нь мөн эх үүсвэр эсвэл эрчим хүч шингээгч (эфир). Yang эсвэл yin.
Исэлдэлтийн зэрэг - Энэ бол "Элсэгдлээс" ойлголттой төстэй ойлголт юм. Энэ нь элементийн редтокс шинж чанарыг тодорхойлдог. Гэхдээ тэдний хооронд дараагийн ялгаа байдаг.
Цахилгаан эрчим хүч нь тусдаа элементийн шинж чанарыг өгдөг. Өөрөө, химийн нэгдэлд үүнийг олохоос гадна. Исэлдэлтийн зэрэг нь Элемент нь ямар ч молекулын нэг хэсэг болоход исэлдүүлэгч, сэргээн засварлах чадварыг тодорхойлдог.
Исэлдүүлэх чадвар гэж юу болохыг бага зэрэг ярилцъя, мөн сэргээх чадвар нь юу вэ гэдгийг бага зэрэг ярилцъя.
Исээх - Энэ бол үнэгүй фотон (электрон) өөр элемент рүү шилжүүлэх үйл явц юм. Expidation нь одоо шинжлэх ухаанд оролцож байгаа гэж үзэж байгаа шиг электронуудыг оруулахгүй. Байна уу. Элемент өөр элементийг исэлдүүлэх үед энэ нь хүчил эсвэл хүчилтөрөгч шиг үйлдэл хийдэг. Исэлдүүлэх - энэ нь устгах, ялзрах, шатаах, шатаах элементүүдийг дэмжих гэсэн үг юм Байна уу. Исэлдүүлэх чадвар нь тэднийг (чөлөөт фотонууд) дамжуулж буй энергийг устгах чадварыг өдөөх чадвар юм. Энэ энерги нь бодисыг үргэлж устгадаг гэдгийг санаарай.
Гайхмаар, шинжлэх ухаанд хэр удаан үргэлжлэх вэ, хэн нэгэнд мэдэгдэхүйц зөрчилдөөн байдаг.
Жишээ нь: "Одоо исэлдүүлэх агент нь электрон агент бол электрон агент бол тэдгээрийг олж авсан бодис нь тэдгээрийг бууруулдаг бодис юм." (Гахайнууд "(Осоль, урвал" -ийг өгдөг бодис юм.
Тэр даруй, доор хоёр догол мөр: "Хамгийн хүчтэй исэлдүүлэгч нь цахилгаан гүйдэл (сөрөг цэнэглэгдсэн электрон)" (IBID.).
Тэдгээртэй. исэн исэлдсэн төлөөлөгч нь электронент агент гэдэг нь электронууд юу шаардагддаг, хоёр дахь исэлдүүлэгч дуудлагад байдаг.
Ижил төстэй алдаатай дүгнэлтүүд нь бие биетэйгээ зөрчилдөж, сургуулиуд, хүрээлэнг дундуур цээжилж өгдөг.
Хамгийн сайн исэлдүүлэгч нь металл биш гэдгийг мэддэг. Түүнээс гадна, үе үе ба түүнээс дээш тооны дугаар, илүү олон бүлгийн дугаар, исэлдүүлэгч нь исэлдүүлэгчийн шинж чанарыг илүү хүчтэй илэрхийлдэг. Энэ нь гайхмаар зүйл биш юм. Энэ нь үе үе дүн шинжилгээний дүн шинжилгээнд хамрагдсаны дагуу, хоёрдугаарт, хоёрдугаар хэсэгт, бөөгнөрөлийн талаар ярьсан. 1-р бүлгээс 8-аас 8 хүртэлх элементүүдийн өнгө, элементүүдийн өнгө нь аажмаар ягаан өнгөөр \u200b\u200bулаан өнгөтэй болж хувирдаг (хэрэв та D- ба F-ийн цэнхэр өнгийн өнгийг) аажмаар сольж байна. Шар, улаан хэсгүүдийн хослол нь хуримтлагдсан үнэгүй фотонуудыг буцааж өгөхийг хөнгөвчилдөг. Шар хуримтлал, гэхдээ сул дорой байгаарай. Улаан нь буцаж ирэхэд хувь нэмэр оруулдаг. Фотонуудыг тавь - энэ бол исэлдэлтийн үйл явц юм. Гэхдээ зарим нь улаан өнгөтэй бол фотон хуримтлуулах боломжтой тоосонцор байхгүй байна. Энэ бол 8 бүлэг, эрхэм жийргэвч нь хөрш, Хөршүүд, галоген шиг ялгаатай биш юм.
Сэргээн босголт - Энэ бол исэлдэлтийн эсрэг үйл явц юм. Одоо, шинжлэх ухааны хувьд химийн элемент нь электроныг хүлээн авахад энэ нь сэргээгдэж байгаа гэдэгт итгэдэг. Энэ үзэл бодлыг ойлгохын тулд үүнийг ойлгох боломжтой (гэхдээ хүлээн авахгүй). Химийн элементийн бүтцийг судлахдаа тэд электроныг ялгаруулдаг болохыг олж мэдсэн. Электронууд нь элементийн нэг хэсэг юм. Энэ нь электрон элементийг шилжүүлэх нь алдагдсан бүтцийг нэг төрлийн, сэргээн засварлах явдал юм гэсэн үг юм.
Гэсэн хэдий ч үнэндээ бүх зүйл буруу байна.
Электронууд үнэгүй фотонууд юм. Тэд цөм биш. Эдгээр нь элементийн биений хэсэг биш юм. Тэд гадаа орж, гадна талд нь нумаа, тэдгээрийн хооронд хуримтлагддаг. Гэхдээ тэдний хуримтлал нь элемент эсвэл молекулын бүтцийг сэргээхэд огт байхгүй. Ялгаатай, эдгээр нь тэдгээрийн ялгаруулалт нь тэдгээрийн элемент (энерги) элементүүдийн холбоосыг сулруулж, устгах, устгах явдал юм. Энэ бол исэлдэлтийн үйл явц, гэхдээ сэргэхгүй байх явдал юм.
Молекулыг сэргээж, бодит байдал дээр сэргээнэ үү, түүнд (энэ тохиолдолд үнэгүй, үнэгүй фотонууд) ав. Фотонуудыг сонгох, элемент сэргээгч бодисыг авсаархан бодисыг авсаардаг - үүнийг сэргээдэг.
Хамгийн сайн бууруулах агентууд металууд юм. Энэхүү өмч нь тэдний чанарын болон тоон найрлагаас хамааран байгалийн жамаар дагаж мөрддөг - тэдний сэтгэл татам байдал нь хамгийн том, гадаргуугийн талбайнууд нь хамгийн том, гадаргуу юм. цэнхэр өнгөний.
Та металыг тодорхойлохыг хүссэн үедээ буцааж авах боломжтой.
Төмөр - Энэ бол Химийн элемент бөгөөд цэнхэр хэсгүүд байх ёстой.
Гэхдээ метал бус - Энэ бол элемент бөгөөд цэнхэр өнгийн давхарга, бараг байхгүй, эсвэл бараг байхгүй, заавал улаан өнгөтэй байх ёстой.
Тэдний хүчтэй сэтгэл татам байдал нь илүү хүчтэйгээр электрон авдаг. Тул тэд агентууд буурч байна.
Бид "ExpoMeCINE" -ийн тодорхойлолтыг "исэлдүүлэх" ойлголтын тодорхойлолтыг "exidation" гэсэн тодорхойлолтыг (ижээний зэрэг "," Redox "-ын зэрэг," Redox "гэсэн ойлголтыг Хими дээрээс олж болно.
« Исэлдэлтийн зэрэг - Энэ нь зөвхөн ионуудаас бүрдсэн гэсэн дүгнэлтээс бүрдсэн нийлбэрээр тооцоолсон нийлбэр дүнгээс хамаарна. Энэ ойлголтыг тодорхойлохдоо энэ нь ердийнхөөрөө (валенент) электронууд илүү электрономон, сөрөг, сөрөг цэнэглэгдсэн байдаг. Исэлдэлтийн зэрэг нь тэг, сөрөг, эерэг утгыг илүүд үздэг.
Исэлдэлтийн зэрэглэлийн тэг утга нь ҮНЭГҮЙ мужид элементийн агуулсан элементийн атомуудтай холбоотой ... exidation Explon Cloud (Encron хос) -ийн сөрөг утгатай. Флюрин нь бүх холболтондоо тэнцүү -1-тэй тэнцүү байна. Эерэг исэлдэл нь өөр атомуудад валентийн электрон өгдөг атомуудтай байдаг. Жишээлбэл, шүлтлэг, шүлтлэг, шүлтлэг дэлхийн металлууд, энэ нь тус тусад нь +1 ба +2. Энгийн ионуудад энэ нь ионы цэнэгтэй тэнцүү юм. Ихэнх нэгдлүүд, устөрөгчийн атомын зэрэг нь + 1, гэхдээ металлууд (устөрөгчтэй) ба бусад нь -1-тэй тэнцүү - энэ нь -1-тэй тэнцүү байна. Хүчилтөрөгчийн хувьд oxiidation -2 зэрэг нь онцлог шинж чанартай, гэхдээ жишигтэй, жишээ нь +2, +2, +2, upoxidation холболтод +2, +2, +2, +2, +2, +2, +2, +2, +2, +2, +2, +2-тэй холболтын хоорондох нэгдэл -1 болно. ...
Нийлмэл атомын иж бүрдэл нь algebraic нийлбэр дүн нь тэг бөгөөд төвөгтэй ион юм. ...
Хамгийн их исэлдэлт бол хамгийн том эерэг утга юм. Ихэнх элементүүдийн хувьд энэ нь үе үе системийн дугаартай тэнцэх бөгөөд холболтын элементийн чухал шинж чанар юм. Электрийн исэлдэлтийн хамгийн бага үнэ цэнэ нь түүний нэгдлүүдийн хэмжээнд тохиолддог бөгөөд тэдгээрийн нэгдлээр нь бага хэмжээгээр исэлдэлт гэж нэрлэгддэг; БУСАД БҮХ - БИДНИЙ ХӨГЖИЛТЭЙ "(Залуу химич, нийтлэл, нийтлэл.
Энэ ойлголттой холбоотой үндсэн мэдээлэл энд байна. Энэ нь өөр нэр томъёотой нягт холбоотой - "Цахилгаан".
« Цахилгаан - Энэ бол химийн бонд үүсэхийн тулд электроныг татахын тулд молекулт атомын чадвар юм "(Залуучуудын химич, нийтлэл" цахилгаан
"Redox-ийн урвал нь урвалын нэг хэсэг болох атомыг expents-ийн нэг хэсэг болох expentation (Reacting Agents (дахин бууруулах агент) исэлдэлтийн болон багасгах урвал, исэлдэх (электрон буцах), сэргээн босгох (электрон нэмэлт) тохиолдох (химийн нэвтэрхий толь толь бичиг) нь (химийн нэвтэрхий толь толь бичиг хэвлэл. I.L. Knunyantz, нийтлэл "редокс урвал").
Бидний бодлоор эдгээр гурван үзэл баримтлалд цөөн хэдэн алдаа гардаг.
Хамгийн эхэнд , Хоёр элементийн хоорондох химийн холболтыг формацийн холболт нь электронизаци хийх бүх үйл явцад байдаггүй гэдэгт бид итгэдэг. Химийн бонд бол таталцлын холболт юм. Цэнэглэгээ, цөмийн эргэн тойронд нисч байгаа гэж үзсэн нь элемент ба тэдгээрийн хоорондох цөмийн гадаргуу дээр хуримтлагдсан фотонууд юм. Хоёр элементийн хооронд холболтын хоорондох тохирохын тулд тэдний үнэгүй фотонууд элементүүдийн хооронд ажиллах шаардлагагүй. Энэ нь тохиолдохгүй. Үнэндээ илүү хүнд элемент нь илүү хөнгөн фотонуудыг сулруулж, татан буулгаж, тэднийг орхиж, тэднийг (илүү нарийвчлалтай) үлдээдэг. Эдгээр фотонуудыг хассан, эсвэл өөр аргаар устгасан илүү хөнгөн элементийн бүс. Энэ бүсэд ямар сэтгэл татам байдаг тул илүү их хэмжээгээр илэрдэг. Илүү хялбар элемент нь ихээхэн татагддаг. Тиймээс химийн бонд гарч ирдэг.
Хоёр хоёралчин , Орчин үеийн химийн бодис нь электронууд нь электронуудыг гажуудуулж буй элементүүдийн чадварыг хардаг. Элементийн электронацац нь электронацацыг илүү том гэж үздэг, тэр илүү ихийг олж авах боломжтой. Мөн хүчилтөрөгчийн флюриныг хамгийн сайн болгодог. Түүнчлэн бусад элементүүд 6, 7 бүлгийн.
Үнэндээ энэ бодол нь төөрөгдөл биш юм. Энэ нь алдаатай харагдац дээр суурилсан бөгөөд илүү их бүлгийн дугаар, илүү хэцүү зүйл юм. Мөн цөмийн эерэгээр эерэгээр нөлөөлнө. Энэ бол Bullshit. Эрдэмтэд өөрсдийн үзэл бодлоос үүдэлтэй гэдгийг тайлбарлахын тулд өөрсдийгөө үймүүлдэггүй. Зүгээр л, тоон дээр дурдсанчлан тэд бүх элементүүдийг дахин тооцоолж, төлбөрийн үнийн тоог харгалзан гарын үсэг зурав. Агуу явган аялал!
Энэ бол нахиа нь өтгөн металлоос хөнгөн байдаг. Химийн хувьд энэ нь хий нь электроныг илүү сайн татдаг гэж үздэг үү?
Өтгөн металлууд, мэдээжийн хэрэг тэд илүү сайн татагддаг.
Мэдээжийн хэрэг, мэдээжийн хэрэг бөгөөд энэ нь "Электронегийн" ойлголтыг мэдээжийн хэрэг бөгөөд энэ нь маш түгээмэл байдаг тул "электрентегийн" ойлголтыг орхиж болно. Гэсэн хэдий ч тэд эсрэг чиглэлд утга учрыг өөрчлөх хэрэгтэй болно.
Цахилгаан - Энэ бол электроныг татахын тулд молекул дахь химийн элементийн чадвар юм. Мөн мэдээж металл дээр, энэ чадвар нь метал бус байдлаас илүү сайн илэрхийлэгддэг.
Молекул дахь цахилгаан шонын хувьд, дараа нь, сөрөг туйл - Эдгээр нь жижиг талбайнуудтай электрон өгдөг төмөр электрон элементүүд юм. Гэхдээ эерэг - Энэ нь илүү ихээр аятайхан металл шинж чанартай байдаг.
Хамт инээмсэглээрэй.
Цахилгаан - Энэ бол бас нэг, эсвэл химийн элементийн чанарыг тодорхойлох өөр нэг оролдлого. Иймд ихэвчлэн тохиолддог, шинжлэх ухааны чиглэлээр мэргэшсэн, химийн чиглэлээр мэргэшсэн хүмүүс, химийн чиглэлээр мэргэшсэн хүмүүс, харин өөрийн хамтрагчдаа итгэж чадахгүй байгаа юм, харин зүгээр л нэг хүн зүгээр л бусдын туршлагыг судлах.
Тиймээс энэ удаад ийм зүйл болсон.
Масс, цэнэг нь бие биентэйгээ харьцахад юу болж байгааг ойлгоход ямар ч хамаагүй химичууд гарч ирэхэд нь ямар ч хамаагүй, Электреончууд нэвтрүүлсэн - Электронегерийг химийн бонд гаргахад оролцсон. Энэ ойлголтын санаа нь маш үнэнийг илэрхийлсэн гэдгийг хүлээн зөвшөөрнө. Энэ нь зөвхөн өөрчлөлтийг урвуу хэлбэртэй хэлбэрээр тусгасан болно. Бидний хэлсэнчлэн Металл бус, гадаргуугийн цөмийн шинж чанарыг сайжруулах нь хамгийн сайн арга юм. Металууд бол хамгийн сайн бууруулах агентууд юм. Үгүй, исэлдүүлэгч бодис. Металлуудыг авч, металл бус өгдөг. Металууд - Yin, NEMMETALLA - YANG.
Эсотерик шинжлэх ухааны хувьд байгалиас шинжлэхэд туслахын тулд шинжлэх ухаанд туслах болно.
Тухай оксияны зэрэг Энэ нь химийн нийлбэр доторх чөлөөт цанилыг хэрхэн тархалт хийх нь сайн оролдлого юм. Молекулууд.
Хэрэв химийн нэгдэл нь жигд, энэ нь энгийн бөгөөд түүний бүтэц нь ижил төрлийн элементүүдээс бүрдэнэ. Дараа нь бүх зүйл үнэн бөгөөд энэ нь үнэний элементүүдээс бүрдэнэ. Энэ холболтонд исэлдүүлэгч байхгүй тул дахин ачаалахгүй байна. Бүх элементүүд нь чанарт тэнцэнэ. Хэн ч электроныг авдаггүй, хэн ч өгдөггүй. Энэ нь өтгөн бодис, шингэн, эсвэл хий эсвэл хий юм уу хий юм.
Исэлдэлтийн зэрэг, мөн цахилгаан электронациас гадна химийн элементийн чанарыг харуулж, зөвхөн химийн элементийн чанарыг харуулж байна. Исэлдэлтийн зэрэг нь нэгтгэсэн химийн элементийн чанарыг харьцуулахад зориулагдсан. Бидний бодлоор энэ санаа сайн байна, гэхдээ түүний хэрэгжилт нь нэлээд сэтгэл хангалуун бус байдаг.
Бид химийн элементүүдийн бүтцийн болон тэдгээрийн хоорондох холболтын бүтцийн болон ойлголтыг бүхэлд нь тодорхойлдог. Тиймээс, зөвхөн миний санааны хувьд үзэж байгаа тул бусад хүмүүсийн тоог 8-аас их байх ёстой. Тиймээс энэхэл бүх үйлчилгээ унтарсан. Тийм ээ, зөвхөн тэгдэггүй. Ерөнхийдөө "Хурууны" атомууд дахь электронуудын тоог дахин тооцоолох нь ямар ч ноцтой биш юм.
Одоогийн концепцийн дагуу хамгийн хүчтэй исэлдүүлэгч нь хамгийн бага зэрэгтэй исэлдэлтийг томилогдсон бөгөөд флюрин нь бүх хэсэг нь бараг хаа сайгүй байдаг. Мөн маш идэвхтэй металлууд - шүлтлэг, шүлтлэг, шүлтлэг, шүлтлэг газар - эдгээр төлбөр, +1 ба +2. Эцсийн эцэст энэ нь туйлын логик биш юм. Хэдийгээр бид давтаж, бид ерөнхийхөө ерөнхий схемийг маш сайн ойлгож, дараа нь хүснэгтэд 8 бүлэгт, гадаад эрчим хүчний түвшинд 8 электрон хэлээр ойлгодог.
Гэсэн хэдий ч, хамгийн бага хэмжээгээр, галоген, хүчилтөрөгчийн хэмжээ, хүчилтөрөгчийн хэмжээ нь хасах тэмдэгтэй хамгийн их байх ёстой байв. Шүлтлэг, шүлтлэг, шүлтлэг металлууд бас том, зөвхөн Plus тэмдэгтэй байдаг.
Аль нь химийн нэгдэл Электронийг өгдөг элементүүд байдаг - expence, металлууд, металлууд, металл, металл, сөрөг цэнэг, электрон, металлууд, металлууд, металлууд, металлууд, эерэг цэнэглэх элементүүд байдаг. Энэ нь элементүүдийг харьцуулах арга бөгөөд тэдгээрийг бие биентэйгээ харьцуулж, бие биенийхээ зэрэгцийг нь тодорхойлох, тэдний исэлдүүлэгчийн зэрэгийг тодорхойлохыг хичээ.
Гэсэн хэдий ч, энэ аргаар exidation-ийн зэрэг, бидний бодлоор, бидний бодлоор бодит байдлыг илэрхийлэх нь тийм ч үнэн зөв байдлыг илэрхийлдэггүй. Молекулын элементийн элементийн электроныг харьцуулах нь илүү зөв байх болно. Эцсийн эцэст, электрентациятаци нь исэлдэлтийн зэрэгтэй бараг ижил байдаг (чанарыг нь тодорхойлдог (чанарыг зөвхөн тусдаа элементээр тодорхойлдог).
Та цахилгаан эрчим хүчийг авч, элемент бүрийн томъёонд оруулж болно. Тэгээд тэр даруй харагдах болно, аль элементүүдийг цахим үзүүлэлтээр харуулах болно. Нэгжийн бүрэлдэхүүн хэсгээс аль нь нэгдмэл байдал нь хамгийн дээд хэмжээ нь хамгийн өндөр нь вэ - сөрөг шон, электрон өгдөг. Цахилгаан тэжээл нь хамгийн жижиг нь хамгийн жижиг нь - эерэг шон, электроныг авдаг.
Хэрэв эд зүйл, хүлээн зөвшөөрөх, молекулад 3, 4 эсвэл 4-ийг хүлээн зөвшөөрөхгүй бол юу ч өөрчлөгддөггүй. Бүгд мөн электрономын чадварыг мөн харьцуулж, харьцуулж үздэг.
Хэдийгээр энэ нь молекулын бүтцийн загварыг зурахаа мартах ёсгүй. Үнэхээр энгийн, энэ нь энгийн биш бол энэ нь энгийн биш, энэ нь нэг төрлийн элементээс бүрдэхгүй бөгөөд энэ нь нэг төрлийн элементээс бүрдэх бөгөөд энэ нь нэг төрлийн элементээс бүрдэхгүй бөгөөд энэ нь нэг төрлийн элементээс бүрдэхгүй бөгөөд энэ нь нэг төрлийн элементээс бүрдэхгүй бөгөөд энэ нь нэг төрлийн элементээс бүрдэхгүй бөгөөд энэ нь нэг төрлийн элементээс бүрдэхгүй бөгөөд энэ нь нэг төрлийн элементээс бүрдэхгүй бөгөөд энэ нь нэг төрлийн элементээс бүрдэхгүй бөгөөд энэ нь нэг төрлийн элементээс бүрдэхгүй бөгөөд энэ нь нэг төрлийн элементээс бүрдүүлдэггүй. Металлууд металл бус электроныг сонгоод, тэдэнд хүлээнэ үү. Мөн металл бус нэг электрон, электронууд 2-ыг нэгэн зэрэг эсвэл илүү тод металл шинж чанартайгээр сонгож болно. Тиймээс нарийн төвөгтэй, нарийн төвөгтэй молекул үүсдэг. Гэхдээ энэ нь ийм молекул, металл элементүүд, металл элементүүд нь хатуу холболт, бие биетэйгээ хамт байх болно гэсэн үг биш юм. Магадгүй тэд бие биенээсээ эсрэг талд байрлах байх. Хэрэв ойрхон байвал - тэд татна. Гэхдээ хатуу холболт нь зөвхөн нэг элемент нь нөгөөгөөсөө илүү металл илүү металл юм. Нэг элементийг нэг элементийг сонгоорой. Үгүй бол элемент нь тохиолдохгүй - гадаргуу дээрх үнэгүй фотоноос чөлөөлөх. Сонирхлын талбар нь бие дааж чадахгүй бөгөөд бат бөх холболт байхгүй болно. уун цогц сэдэв - боловсрол хИМИЙН ҮЙЛДВЭРЭнэ нийтлэлд энэ талаар дэлгэрэнгүй ярихгүй.
Бид "ExploneCINICE" гэсэн ойлголтыг маш ихээр асааж, "исэлдэлт", "исэлдэлт", "исэлдэлт", "Excoration", "СУРГАЛТ" -ийн тухай ойлголт, "Сэргээх" ойлголтыг анзаарсан бөгөөд анхаарлаа хандуулаарай.
Номын удирддаг мөрөөдлөөс Дэлхийн Елена зохиогчСэргээх "Indi-Appeam-ийн нэгдсэн шинж тэмдэг төрөх үед, мөн чанар, мөн чанар, амьдрал хоёр хуваагдана. Хэрэв энэ үеэс эхлэн, хэрэв эцсийн ертөнцөд хүрэхгүй бол мөн чанар, мөн чанар, амьдрал бие биенээ хэзээ ч харахгүй. " Институтын дараа "алтан цэцгийн нууцлаг байдал"
Нууцын номноос. Гадаадад болон гадаадад гайхалтай Зохиолч Vyatkin arkady dmitriveichЭнэхүү утгаараа Masochism нь энэхүү утгаараа маш сайн дурын хэм хэмжигдэхүүн юм. Masochism нь харилцаа холбоо нь харилцаа холбоо юм. Mazochists бол өөрсдийн бие махбодийн болон сэтгэлийн зовлонгоос аятайхан мэдрэмжийг авдаг хүмүүс юм. Өөрөөр хэлбэл тэд зодож, загнахдаа дуртай, шоолох дуртай
Орос дахь номын вампируудаас. Та тэдний талаар мэдэх хэрэгтэй! Зохиолч Бауэр АлександрЦус сорогч цус уух үед цус алдах цусны зөрчлийг хэрхэн тодорхойлох вэ, дараа нь хагас литрээс нэг литрийг нэг литр цусны дараа ууна. Хүний бие нь ердөө тав, зургаан литр цусыг агуулдаг тул ийм цус алдах нь амьдралд аюултай байх албагүй. Гэсэн хэдий ч цус сорогч лаазалдаг
Мөрөөдлийнхөө ирээдүйд ирээдүйг загварчлах тухай Дэлхийн Елена зохиогчИнститутын тархалтын дараа сэргээж, хаалттай компанид инженерээр ажиллаж байгаа бөгөөд би өөрийнхөө оронд биш байсан бөгөөд би мэргэжлээ өөрчлөх гэж байгаагаа, дараа нь ангийн сургалтын сургуульд сурч мэдсэн, дараа нь сонгодог оффисын сургуульд сурч мэдсэн бөгөөд дараа нь хөгжмийн оффисын сургуульд сурч мэдсэн Байна уу.
Номын алтан дүрмээс FENGSHUI. Амжилтанд хүрэх 10 энгийн алхам, сайн сайхан байдал, урт наслалт Зохиолч Рудин Валентин ЛеонидовичГадаад объектуудын сөрөг нөлөөллийн зэрэг нь хамгийн их сөрөг нөлөөтэй гадаад объектууд байшинд орохоос өмнө нэн даруй байх ёстой. Гэхдээ тэд илүү их байр суурин дээр байрладаг бөгөөд сул дорой байдал нь тэдний нөлөөлөл болж хувирдаг. Обьект шууд байна
Зохиолч Эдуард эмчлэх замаарНэгдүгээр зэрэг: Хоол хийх. Нейнни Кермон ба Бурханы хатан хаан Христийн хаант улс Галилейгийн Вантили ба Галили Тодир, зарлалаас эхэлдэг. Энэхүү таамаглал нь бидэнд түгээмэл зааврыг илтгэнэ. Үүний зэрэгцээ энэ нь илүү өндөрлөгт бэлтгэх явдал юм
Номноос хувьсал. Сфинксээс Христ хүртэл Зохиолч Эдуард эмчлэх замаарСанал болгож буй хоёрдугаар зэргийн (цэвэрлэх). Гайхамшигтай эдгэрэлт. Ёс суртахууны болон оюуны бэлтгэлд зориулсан Христийн Эмчилгээний эмч нар Ёс суртахууны эмчилгээнд, энэ нь шинэ эрхтнүүдийг сэргээхийн тулд сэтгэлийг цэвэрлэж, энэ нь шинэ эрхтнүүдийг сэргээх ёстой байсан
Номноос том sphinx оньсого Зохиолч Барбарен ГебаруудХөшүүргийг сэргээх нь том sphinx-ийн бодит насыг сэргээх нь Адам Эрагийн эхэнд буцаж очно. Наад зах нь тэр бол орчин үеийн пирамид, түүний харж, түүнийг харж, дуусгасан. Том SPHYNX-ийн дүр төрх
Сэтгэлийг эдгээх номноос. 100 Бясалгалын бясалгалын техник, эдгэрэлт, эдгэрэлт, амралт Зохиолч Ражниш Бхагван ШриХэмнэлийг сэргээх ... Орой руу орохын тулд нэг удаа суулгана уу. Хэрэв орой нь арван нэгэн бол энэ нь арван нэгэн бөгөөд энэ нь тодорхой цаг хугацаа гэсэн үг юм. ЭНЭ ЦАГДААГҮЙ БОЛОХГҮЙ, ҮНЭГҮЙ БОЛОМЖТОЙ БОЛОМЖТОЙ БОЛОМЖТОЙ. Биеийн
Зохиогч Kuzmishin E. L.Оюутны зэрэгт оюутны хүлээн авалт. Lodge-ийн голд, байрны чимэглэл, rodge-ийн чимэглэл, таазыг ЖИЛИЙН ХӨДӨЛГӨӨНИЙ ТУХАЙ ХОЛБООНЫ ТУХАЙ, БИДНИЙ ТУХАЙ. Шинжээчдийн толгойн дээгүүр нь түүний төвд байгаа нэртэй гурвалжны гялалзсан гялалзсан замаар хүрээлэгдсэн байдаг
Калиосостро ба Египетэд Мастетчуудын номноос Зохиогч Kuzmishin E. L.Оюутны зэрэгт хүлээн авах. Лоджестын голд ба домэйн ба таазыг цоорхойгүйгээр цэнхэр, цагаан өнгөтэй байх ёстой. Шинжээчдийн эзний толгой дээр нь "Ехова" гэдэг нь "Ехова" -тай хамт гурвалжингаар хүрээлэгдсэн замаар хүрээлэгдсэн байдаг
Номын намтар йога Зохиолч Йогананда парамиансаБүлэг 23 Би их сургуулийн зэрэг авдаг - та сурах бичигт гүнзгий тодорхойлолтыг үл тоомсорлож байгаа нь танд бүх шалгалтаар дамжуулж байна. Гэхдээ та яаралтай тусламжийн талаар нэн даруй зөвлөдөггүй бол би тэгэх хэрэгтэй болно
Каббалагийн номноос. Хамгийн өндөр ертөнц. Арга замын эхлэл Зохиолч Lightman Michael.7.5. "Тарчлал" гэсэн ойлголтыг "тарчлах" гэсэн ойлголтын зэрэг, таашаал, аз жаргал, зовлон зүдүүрийн ижил төстэй байдал, таашаал, тэвчээргүй байдал, тэвчээргүй байдал, Үүний дагуу, Эгоизм нь бидэнд болон тэвчих чадваргүй будаг юм.
Сонголт 1
1. Дараах холболтонд химийн элементийн ocomation-ийн ижмийн хэмжээг тодорхойлно уу: HNO₃, NON, H₃N, SON, N₂O.
2. Тоглоомын хүснэгтийн давуу талыг ашиглахын тулд EncromoneGInity-ийг багасгахын тулд дараахь элементүүдийг ашиглана уу: o, n, be, b, li, c. Хариултыг тайлбарлана уу. 
3. Сульфурын атомын зэрэг нь хэрүүл хэрхэн яаж өөрчлөгдөх вэ? Хариултаа тайлбарлана уу.
Сонголт 2.
1. Дараах холболтонд химийн элементийн ижмийн агентуудын зэрэг олгох: CO₂, HIFO, HIFO, SIH₄, P₂O₅, MG₂SI.
2. Химийн элементийг ерөнхийдөө шилжүүлсэн атомын чиглэлд цооног хос, Дараах холболтын молекулууд: BF₃, PCL₃, CS₂, CS₂, CCL₄, HBRO? Боломжийн хариулт өгөх.
3. Формацийн үед нүүрстөрөгчийн исэлдүүлэгч өөрчлөлтийн зэрэг ногоон угаана H₂co₃ нүүрстөрөгчийн давхар исэл, ус уу? Хариултаа тайлбарлана уу.
Сонголт 3.
1. Дараах холболтонд химийн элементийн ижмийн агентуудын зэрэг хамгааллын зэрэг: CL₂, NACLO, CACLO, CACLO, CACLO, CL₂o₇.
2. ашиглах дараах тогтоол Химийн элементүүд, дараахь элементүүдийг цахилгаан чадвараа нэмэгдүүлэх дарааллаар байрлуулна: P, AL, AL, CL, NA, S, MG, MG. Энэ мөрөнд кали, фторыг олоорой. Хариултаа тайлбарлана уу. 
3. Метаны исэл нь нүүрстөрөгчийн исэл (IV), усыг шатаахад метаны исэл хэрхэн яаж ажилладаг вэ? Хариултаа тайлбарлана уу.
Сонголт 4.
1. Дараах холболтонд химийн элементийн acenes-ийн ижмийн хэмжээг тодорхойл: H₂so₄, o₂, bf₃, h₂s.
2. Атомуудад чиглэсэн химийн элементүүд Ерөнхий цахим хосыг харуулна: H₂o, PCL₃, HACLE, H₃N, H₂S, COIN? Боломжийн хариулт өгөх.
3. Ус өөрчлөгдөх үед атомын градаж байгаа эсэх энгийн бодисууд - устөрөгч ба хүчилтөрөгч үү? Хариултаа тайлбарлана уу.


