อิเล็กโทรเนกาติวิตีเป็นสมบัติขององค์ประกอบทางเคมีในการดึงดูดอิเล็กตรอนมายังอะตอมของมันจากอะตอมของธาตุอื่น ๆ ซึ่งองค์ประกอบนี้ก่อให้เกิดพันธะเคมีในสารประกอบ
เมื่อเกิดพันธะเคมีระหว่างอะตอมของธาตุที่แตกต่างกันเมฆอิเล็กตรอนทั่วไปจะเปลี่ยนไปเป็นอะตอมอิเล็กโทรเนกาติวิตีมากขึ้นเนื่องจากพันธะกลายเป็นขั้วโควาเลนต์และด้วยความแตกต่างของอิเล็กโทรเนกาติวิตีไอออนิก
อิเล็กโทรเนกาติวิตีถูกนำมาพิจารณาเมื่อเขียนสูตรทางเคมี: ในสารประกอบไบนารีสัญลักษณ์ขององค์ประกอบอิเล็กโทรเนกาติวิตีส่วนใหญ่จะถูกเขียนไว้ข้างหลัง
อิเล็กโทรเนกาติวิตีเพิ่มขึ้นจากซ้ายไปขวาสำหรับองค์ประกอบของแต่ละช่วงเวลาและลดลงจากบนลงล่างสำหรับองค์ประกอบในกลุ่ม PS เดียวกัน
วาเลนซ์ องค์ประกอบคือคุณสมบัติของอะตอมที่จะรวมกับอะตอมอื่น ๆ จำนวนหนึ่ง
แยกแยะระหว่างสโตอิชิโอเมตริกความจุอิเล็กทรอนิกส์และหมายเลขโคออร์ดิเนชัน เราจะพิจารณาเฉพาะความจุแบบสโตอิชิโอเมตริกเท่านั้น
Stoichiometric วาเลนซ์แสดงจำนวนอะตอมของธาตุอื่นที่ติดอยู่โดยอะตอมขององค์ประกอบนี้ หน่วยวาเลนซ์ถูกนำมาเป็นความจุไฮโดรเจนตั้งแต่ ไฮโดรเจนเป็นโมโนวาเลนต์เสมอ ตัวอย่างเช่นในสารประกอบ HCl, H 2 O, NH 3 (การสะกดที่ถูกต้องของแอมโมเนีย H 3 N มีใช้อยู่แล้วในคู่มือสมัยใหม่) คลอรีน CH 4 เป็นโมโนวาเลนต์ออกซิเจนเป็นดิวาเลนต์ไนโตรเจนเป็นไตรวาเลนต์และคาร์บอนเป็นเตตราวาเลนต์
โดยทั่วไปความจุของออกซิเจนจะเป็น 2 เนื่องจากองค์ประกอบเกือบทั้งหมดรวมตัวกันเป็นสารประกอบกับออกซิเจนจึงสะดวกที่จะใช้เป็นข้อมูลอ้างอิงเพื่อกำหนดความจุขององค์ประกอบอื่น ตัวอย่างเช่นในสารประกอบ Na 2 O, CoO, Fe 2 O 3, SO 3 โซเดียมคือโมโนวาเลนต์โคบอลต์เป็นดิวาเลนต์เหล็กเป็นไตรวาเลนต์กำมะถันเป็นเฮกซะวาเลนต์
ในปฏิกิริยารีดอกซ์สิ่งสำคัญสำหรับเราในการกำหนดสถานะออกซิเดชันของธาตุ
สถานะออกซิเดชั่น องค์ประกอบในสสารเรียกว่า stoichiometric valence โดยใช้เครื่องหมายบวกหรือลบ
องค์ประกอบทางเคมีแบ่งย่อยออกเป็นองค์ประกอบ ความจุคงที่ องค์ประกอบของความจุตัวแปร
1.3.3. สารโครงสร้างโมเลกุลและไม่ใช่โมเลกุล ชนิดขัดแตะคริสตัล. การพึ่งพาคุณสมบัติของสารต่อองค์ประกอบและโครงสร้าง
ขึ้นอยู่กับสถานะของสารประกอบในธรรมชาติพวกมันถูกแบ่งออกเป็นโมเลกุลและไม่ใช่โมเลกุล ใน สารโมเลกุล อนุภาคโครงสร้างที่เล็กที่สุดคือโมเลกุล สารเหล่านี้มีตาข่ายผลึกโมเลกุล ในสารที่ไม่ใช่โมเลกุลอนุภาคโครงสร้างที่เล็กที่สุดคืออะตอมหรือไอออน โครงตาข่ายคริสตัลของพวกเขาคืออะตอมไอออนิกหรือโลหะ
ชนิดของตาข่ายคริสตัลส่วนใหญ่กำหนดคุณสมบัติของสาร ตัวอย่างเช่นโลหะที่มี ตาข่ายคริสตัลชนิดโลหะแตกต่างจากองค์ประกอบอื่น ๆ ทั้งหมด ความเป็นพลาสติกสูงการนำไฟฟ้าและความร้อน... คุณสมบัติเหล่านี้เช่นเดียวกับคุณสมบัติอื่น ๆ อีกมากมาย - ความสามารถในการอ่อนตัวความมันวาวของโลหะ ฯลฯ เนื่องจากพันธะพิเศษระหว่างอะตอมของโลหะ - การเชื่อมต่อโลหะ ควรสังเกตว่าคุณสมบัติที่มีอยู่ในโลหะจะปรากฏเฉพาะในสถานะที่ควบแน่นเท่านั้น ตัวอย่างเช่นเงินที่อยู่ในสถานะก๊าซไม่มีคุณสมบัติทางกายภาพของโลหะ
พันธะพิเศษในโลหะ - โลหะ - เกิดจากการขาดเวเลนซ์อิเล็กตรอนดังนั้นจึงเป็นเรื่องธรรมดาสำหรับโครงสร้างทั้งหมดของโลหะ แบบจำลองโครงสร้างของโลหะที่ง่ายที่สุดสันนิษฐานว่าโครงตาข่ายคริสตัลของโลหะประกอบด้วยไอออนบวกที่ล้อมรอบด้วยอิเล็กตรอนอิสระการเคลื่อนที่ของอิเล็กตรอนจะเกิดขึ้นอย่างวุ่นวายเช่นเดียวกับโมเลกุลของก๊าซ อย่างไรก็ตามแบบจำลองดังกล่าวในขณะที่อธิบายคุณสมบัติหลายประการของโลหะในเชิงคุณภาพ แต่กลับกลายเป็นว่าไม่เพียงพอในการตรวจสอบเชิงปริมาณ การพัฒนาทฤษฎีสถานะโลหะเพิ่มเติมนำไปสู่การสร้าง ทฤษฎีโซนของโลหะซึ่งเป็นไปตามแนวคิดของกลศาสตร์ควอนตัม
ในโหนดของโครงตาข่ายคริสตัลมีไอออนบวกและอะตอมของโลหะและอิเล็กตรอนเคลื่อนที่ไปตามโครงตาข่ายคริสตัลได้อย่างอิสระ
คุณสมบัติเชิงกลของโลหะคือ พลาสติกเนื่องจากลักษณะเฉพาะของโครงสร้างภายในของผลึก ความเป็นพลาสติกถูกเข้าใจว่าเป็นความสามารถของร่างกายภายใต้อิทธิพลของแรงภายนอกในการรับการเปลี่ยนรูปซึ่งยังคงอยู่แม้หลังจากการสิ้นสุดของอิทธิพลภายนอก คุณสมบัติของโลหะนี้ช่วยให้สามารถขึ้นรูปเป็นรูปร่างต่างๆได้ในระหว่างการตีขึ้นรูปรีดเป็นแผ่นหรือลากเป็นเส้นลวด
ความเป็นพลาสติกของโลหะเกิดจากความจริงที่ว่าภายใต้อิทธิพลภายนอกชั้นของไอออนที่ก่อให้เกิดการเปลี่ยนแปลงของโครงตาข่ายคริสตัลที่สัมพันธ์กันโดยไม่มีการแตก สิ่งนี้เกิดขึ้นจากข้อเท็จจริงที่ว่าอิเล็กตรอนที่ถูกแทนที่เนื่องจากการกระจายแบบอิสระยังคงสื่อสารระหว่างชั้นไอออนิกต่อไป ภายใต้การกระทำทางกลบนของแข็งที่มีตาข่ายอะตอมแต่ละชั้นจะถูกแทนที่และการยึดเกาะระหว่างพวกมันจะแตกเนื่องจากการแตก พันธะโควาเลนต์.
ไอออนจากนั้นสารเหล่านี้ก่อตัวขึ้น ตาข่ายคริสตัลชนิดไอออนิก.

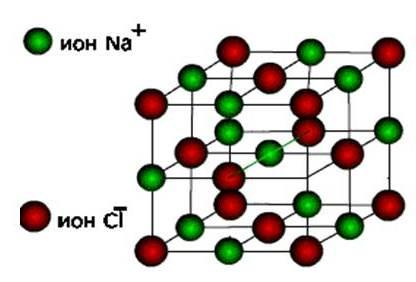
สิ่งเหล่านี้คือเกลือเช่นเดียวกับออกไซด์และไฮดรอกไซด์ของโลหะทั่วไป สารเหล่านี้เป็นสารที่แข็งและเปราะบาง แต่มีคุณภาพหลัก : สารละลายและการละลายของสารประกอบเหล่านี้นำกระแสไฟฟ้า.
หากไซต์ของคริสตัลขัดแตะนั้น อะตอมจากนั้นสารเหล่านี้ก่อตัวขึ้น ประเภทอะตอมของตาข่ายคริสตัล(เพชรโบรอนซิลิคอนออกไซด์ของอลูมิเนียมและซิลิกอน) มีคุณสมบัติแข็งและทนไฟไม่ละลายในน้ำ
หากไซต์ของคริสตัลขัดแตะนั้น โมเลกุลจากนั้นสารเหล่านี้จะก่อตัวขึ้น (ภายใต้สภาวะปกติก๊าซและของเหลว: О 2, HCl; I 2 อินทรียฺวัตถุ).
เป็นที่น่าสนใจที่จะสังเกตเห็นแกลเลียมโลหะซึ่งละลายที่อุณหภูมิ 30 o C ความผิดปกตินี้อธิบายได้จากข้อเท็จจริงที่ว่าโมเลกุล Ga 2 อยู่ในโหนดของโครงตาข่ายคริสตัลและคุณสมบัติของมันซึ่งคล้ายกับสารที่มี a ตาข่ายคริสตัลโมเลกุล
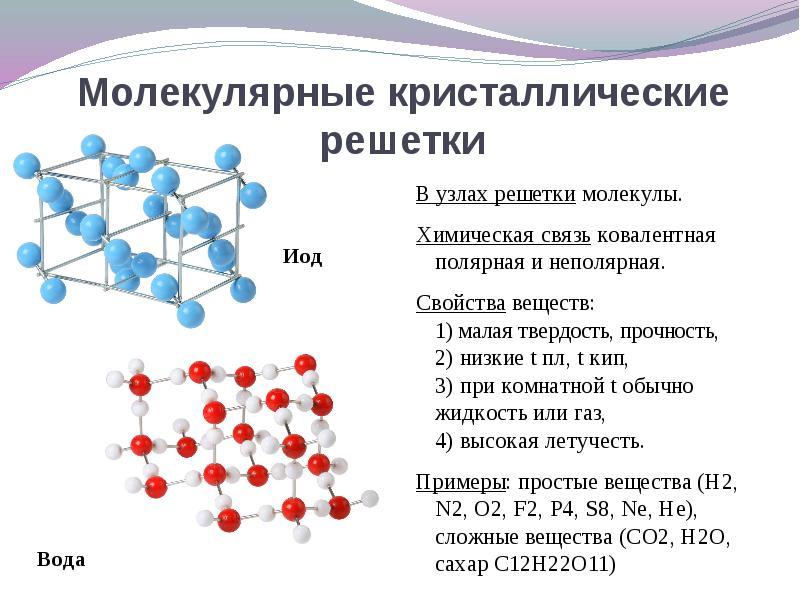
ตัวอย่าง.อโลหะทั้งหมดในกลุ่มมีโครงสร้างที่ไม่ใช่โมเลกุล:
1) คาร์บอนโบรอนซิลิคอน 2) ฟลูออรีนโบรมีนไอโอดีน;
3) ออกซิเจนกำมะถันไนโตรเจน 4) คลอรีนฟอสฟอรัสซีลีเนียม
ในสารที่ไม่ใช่โมเลกุลอนุภาคโครงสร้างที่เล็กที่สุดคืออะตอมหรือไอออน โครงตาข่ายคริสตัลเป็นอะตอมไอออนิกหรือโลหะ
เมื่อไหร่ การตัดสินใจ คำถามนี้ง่ายกว่าที่จะไปจากตรงข้าม หากไซต์ของคริสตัลขัดแตะนั้น โมเลกุลจากนั้นสารเหล่านี้ก่อตัวขึ้น ประเภทโมเลกุลของตาข่ายคริสตัล(ภายใต้สภาวะปกติก๊าซและของเหลว: O 2, HCl; เช่นกัน I 2, ขนมเปียกปูนกำมะถัน S 8, ฟอสฟอรัสขาว P 4, สารอินทรีย์) ตามคุณสมบัติของพวกมันเหล่านี้เป็นสารประกอบที่หลอมละลายต่ำที่เปราะบาง
ในคำตอบที่สองคือก๊าซฟลูออรีนในก๊าซออกซิเจนและไนโตรเจนที่สามในก๊าซคลอรีนที่สี่ ซึ่งหมายความว่าสารเหล่านี้มีโครงตาข่ายคริสตัลโมเลกุลและโครงสร้างโมเลกุล
ใน อันดับแรก คำตอบคือสารทั้งหมดเป็นสารประกอบที่เป็นของแข็งภายใต้สภาวะปกติและก่อตัวเป็นตาข่ายอะตอมซึ่งหมายความว่าสารเหล่านี้มีโครงสร้างที่ไม่ใช่โมเลกุล
คำตอบที่ถูกต้อง:1) คาร์บอนโบรอนซิลิคอน
- องค์ประกอบทางเคมีที่มีอิเล็กโทรเนกาติวิตีน้อยที่สุดคือ
- เหล็ก
- แมกนีเซียม
- แคลเซียม
ควรให้ความสนใจกับวลี "อิเล็กโทรเนกาติวิตีน้อยที่สุด" นั่นคือองค์ประกอบที่มีคุณสมบัติเป็นโลหะมากที่สุด ข้อโต้แย้งนี้จะช่วยให้เราสามารถแยกไนโตรเจนออกจากคำตอบที่เป็นไปได้ในฐานะที่เป็นอโลหะและมุ่งเน้นไปที่แคลเซียมเป็นโลหะที่มีการใช้งานมากที่สุดที่เสนอในงาน คำตอบ: 4.
- พันธะเคมีที่มีขั้วมากที่สุดในโมเลกุลใดโมเลกุลหนึ่ง
- CCl 4
- CBr 4
ความรู้เกี่ยวกับความสม่ำเสมอของการเปลี่ยนแปลงอิเล็กโตรเนกาติวิตีในช่วงเวลาและกลุ่มของตารางธาตุ D.I. คำตอบ: 2.
- ในโมเลกุลของไฮโดรเจนคลอไรด์และคลอรีนพันธะเคมีตามลำดับ
- ขั้วไอออนิกและโควาเลนต์
- ไอออนิกและโควาเลนต์ไม่มีขั้ว
- โควาเลนต์มีขั้วและโควาเลนต์ไม่มีขั้ว
- ไฮโดรเจนและโควาเลนต์ไม่มีขั้ว
คำสำคัญสำหรับการทำงานนี้ให้เสร็จอย่างรวดเร็วและถูกต้องคือ "ตามนั้น" ในตัวแปรที่เสนอมีเพียงคำตอบเดียวที่ขึ้นต้นด้วยคำว่า "โควาเลนต์โพลาร์" นั่นคือลักษณะพันธะของไฮโดรเจนคลอไรด์ คำตอบ: 3.
- สถานะออกซิเดชันของแมงกานีสในสารประกอบที่มีสูตรคือ K 2 MnO 4 คือ
การรู้กฎสำหรับการคำนวณสถานะออกซิเดชันขององค์ประกอบโดยสูตรจะช่วยให้คุณสามารถเลือกคำตอบที่ถูกต้องได้ คำตอบ: 3.
- กำมะถันในเกลือมีสถานะออกซิเดชั่นต่ำที่สุด
- โพแทสเซียมซัลเฟต
- โพแทสเซียมซัลไฟต์
- โพแทสเซียมซัลไฟด์
- โพแทสเซียมไฮโดรเจนซัลไฟด์
เห็นได้ชัดว่าการทำให้งานนี้เสร็จสิ้นอย่างรวดเร็วจะอำนวยความสะดวกโดยการแปลชื่อของเกลือเป็นสูตร เนื่องจากกำมะถันเป็นองค์ประกอบของกลุ่ม VIA สถานะออกซิเดชั่นต่ำสุดคือ -2 ค่านี้สอดคล้องกับสารประกอบที่มีสูตร K 2 S - โพแทสเซียมซัลไฟด์ คำตอบ: 3.
- สถานะออกซิเดชั่น +5 อะตอมของคลอรีนมีอยู่ในไอออน
- C1O - 4
- C1O -
- C1O - 3
- C1O - 2
เมื่อปฏิบัติภารกิจนี้คุณควรใส่ใจกับข้อเท็จจริงที่ว่าในสภาพนี้จะไม่มีสารประกอบที่เป็นกลางทางไฟฟ้า แต่เป็นไอออนของคลอรีนที่มีประจุลบเพียงครั้งเดียว ("-") เนื่องจากผลรวมของสถานะออกซิเดชันของอะตอมในไอออนเท่ากับประจุของไอออนประจุลบทั้งหมดของอะตอมออกซิเจนในไอออนที่ต้องการควรมีค่า -6 (+5 - 6 \u003d -1) คำตอบ: 3.
- สถานะออกซิเดชั่น -3 ไนโตรเจนมีอยู่ในสารประกอบทั้งสอง
- NF 3 และ NH 3
- NH 4 Cl และ N 2 O 3
- NH 4 Cl และ NH 3
- HNO 2 และ NF 3
ในการพิจารณาคำตอบที่ถูกต้องคุณต้องแบ่งตัวเลือกคำตอบออกเป็นคอลัมน์ย่อยด้านซ้ายและด้านขวา จากนั้นเลือกสารประกอบที่มีองค์ประกอบที่ง่ายกว่า - ในกรณีของเรานี่คือคอลัมน์ย่อยทางขวาของสารประกอบไบนารี การวิเคราะห์จะช่วยให้เราไม่รวมคำตอบที่ 2 และ 4 เนื่องจากในไนโตรเจนออกไซด์และฟลูออไรด์มีสถานะออกซิเดชั่นเป็นบวกเช่นเดียวกับธาตุอิเล็กโทรเนกาติวิตี อาร์กิวเมนต์นี้ช่วยให้เราไม่รวมคำตอบ 1 เนื่องจากสารแรกในนั้นคือไนโตรเจนฟลูออไรด์เดียวกัน คำตอบ: 3.
- เพื่อให้สาร โครงสร้างโมเลกุล ไม่ใช้
- คาร์บอนไดออกไซด์
- มีเทน
- ไฮโดรเจนคลอไรด์
- แคลเซียมคาร์บอเนต
คุณควรใส่ใจกับการตัดสินเชิงลบที่มีอยู่ในเงื่อนไขของงาน เนื่องจากสารที่เป็นก๊าซภายใต้สภาวะปกติมีตาข่ายผลึกโมเลกุลในสถานะของแข็งตัวเลือก 1-3 จึงไม่เป็นไปตามเงื่อนไขของงาน การกำหนดแคลเซียมคาร์บอเนตให้กับเกลือจะเป็นการยืนยันคำตอบที่ถูกต้องอีกครั้ง คำตอบ: 4.
- คำตัดสินต่อไปนี้เกี่ยวกับคุณสมบัติของสารและโครงสร้างถูกต้องหรือไม่?
A. ผ้าเปียกจะแห้งในน้ำค้างแข็งเนื่องจากสารที่มีโครงสร้างโมเลกุลสามารถระเหิดได้ (sublimation)
B. ผ้าเปียกแห้งในความเย็นเนื่องจากโมเลกุลของน้ำมีน้ำหนักโมเลกุลต่ำ
- a เท่านั้นที่เป็นจริง
- b เท่านั้นที่เป็นจริง
- คำตัดสินทั้งสองถูกต้อง
- คำตัดสินทั้งสองไม่ถูกต้อง
ความรู้ คุณสมบัติทางกายภาพ สารที่มีโครงสร้างโมเลกุลช่วยให้เราตัดสินใจได้ว่าสาเหตุที่ทำให้เสื้อผ้าเปียกแห้งในความเย็นคือความสามารถของน้ำแข็งในการระเหิดไม่ใช่โครงสร้างไดโพลของโมเลกุลของน้ำ คำตอบ: 1.
- สารแต่ละชนิดมีโครงสร้างโมเลกุลซึ่งเป็นสูตรที่ระบุไว้ในชุดข้อมูล
- CO 2, HNO 3, CaO
- นา 2 S, Br 2, NO 2
- H 2 SO 4, Cu, O 3
- ดังนั้น 2, ฉัน 2, HCl
เนื่องจากตัวเลือกที่เสนอมีสามสารแต่ละชนิดจึงมีเหตุผลที่จะแบ่งตัวเลือกเหล่านี้ออกเป็นสามเสาหลักในแนวตั้ง การวิเคราะห์แต่ละรายการโดยเริ่มจากสารที่มีองค์ประกอบที่เรียบง่ายกว่า (เสากลาง) จะช่วยให้เราไม่รวมคำตอบที่ 3 เนื่องจากประกอบด้วยโลหะทองแดงซึ่งมีตาข่ายคริสตัลโลหะ การวิเคราะห์คอลัมน์ย่อยด้านขวาที่คล้ายกันจะช่วยให้เราไม่รวมคำตอบที่ 1 เนื่องจากประกอบด้วยออกไซด์ของโลหะอัลคาไลน์เอิร์ ธ (ตาข่ายไอออนิก) จากสองตัวเลือกที่เหลือจะต้องยกเว้นตัวเลือกที่ 2 เนื่องจากมีเกลือโลหะอัลคาไล - โซเดียมซัลไฟด์ (ตาข่ายไอออนิก) คำตอบ: 4.
งานศึกษาด้วยตนเอง
- สถานะออกซิเดชั่น +5 ไนโตรเจนแสดงอยู่ในสารประกอบซึ่งมีสูตรคือ
- ไม่มี 2 O 5
- ไม่มี 2 O 4
- N 2 O
- สถานะออกซิเดชันของโครเมียมในสารประกอบที่มีสูตร (NH 4) 2 Cr 2 O 7 คือ
- สถานะออกซิเดชันของไนโตรเจนจะลดลงในสารหลายชนิดซึ่งเป็นสูตรที่
- NH 3, ไม่ 2, KNO 3
- N 2 O 4, KNO 2, NH 4 Cl
- N 2, N 2 O, NH 3
- HNO 3, HNO 2, NO 2
- สถานะออกซิเดชั่นของคลอรีนจะเพิ่มขึ้นในสารหลายชนิดซึ่งเป็นสูตรที่
- НСlO, НСlO 4, КСlO 3
- Сl 2, С1 2 O 7, КСlO 3
- Ca (C1O) 2, KClO 3, HClO 4
- КСl, КСlO 3, КСlO
- พันธะเคมีที่มีขั้วมากที่สุดในโมเลกุล
- แอมโมเนีย
- ไฮโดรเจนซัลไฟด์
- ไฮโดรเจนโบรไมด์
- ไฮโดรเจนฟลูออไรด์
- สารที่มีพันธะโควาเลนต์ไม่มีขั้ว
- ฟอสฟอรัสขาว
- อลูมิเนียมฟอสไฟด์
- ฟอสฟอรัส (V) คลอไรด์
- แคลเซียมฟอสเฟต
- สูตรของสารที่มีพันธะไอออนิกเท่านั้นจะถูกเขียนในแถว
- โซเดียมคลอไรด์ฟอสฟอรัส (V) คลอไรด์โซเดียมฟอสเฟต
- โซเดียมออกไซด์โซเดียมไฮดรอกไซด์โซเดียมเปอร์ออกไซด์
- คาร์บอนไดซัลไฟด์แคลเซียมคาร์ไบด์แคลเซียมออกไซด์
- แคลเซียมฟลูออไรด์แคลเซียมออกไซด์แคลเซียมคลอไรด์
- ตาข่ายคริสตัลอะตอมมี
- โซเดียมออกไซด์
- แคลเซียมออกไซด์
- ซัลเฟอร์ (IV) ออกไซด์
- อลูมิเนียมออกไซด์
- การเชื่อมต่อไอออนิก ตาข่ายคริสตัล เกิดขึ้นจากปฏิสัมพันธ์ของคลอรีนกับ
- ฟอสฟอรัส
- แบเรียม
- ไฮโดรเจน
- สีเทา
- คำตัดสินต่อไปนี้เกี่ยวกับแอมโมเนียมคลอไรด์ถูกต้องหรือไม่?
A. แอมโมเนียมคลอไรด์ - สารที่มีโครงสร้างไอออนิกซึ่งเกิดขึ้นเนื่องจากพันธะโควาเลนต์และขั้วไอออนิก
บีแอมโมเนียมคลอไรด์ - สารที่มีโครงสร้างไอออนิกดังนั้นจึงเป็นของแข็งทนไฟและไม่ระเหย
- a เท่านั้นที่เป็นจริง
- b เท่านั้นที่เป็นจริง
- คำตัดสินทั้งสองถูกต้อง
- การตัดสินทั้งสองผิด
08. อิเล็กโทรเนกาติวิตี, สถานะออกซิเดชั่น, ออกซิเดชั่นและรีดักชัน
มาพูดถึงความหมายของแนวคิดที่น่าสนใจอย่างยิ่งที่มีอยู่ในวิชาเคมีและมักเป็นกรณีทางวิทยาศาสตร์ที่ค่อนข้างสับสนและใช้กลับหัว เราจะพูดถึง "อิเล็กโทรเนกาติวิตี" "สถานะออกซิเดชั่น" และ "ปฏิกิริยารีดอกซ์"
หมายความว่าอย่างไร - แนวคิดนี้ใช้กลับหัว?
เราจะพยายามเล่าให้คุณฟังอย่างค่อยเป็นค่อยไป
อิเล็กโทรเนกาติวิตี แสดงให้เราเห็นคุณสมบัติรีดอกซ์ขององค์ประกอบทางเคมี นั่นคือความสามารถในการรับหรือให้โฟตอนฟรี และองค์ประกอบนี้เป็นแหล่งหรือตัวดูดซับพลังงาน (อีเธอร์) หรือไม่ หยางหรือหยิน
สถานะออกซิเดชั่น เป็นแนวคิดที่คล้ายกับอิเล็กโทรเนกาติวิตี นอกจากนี้ยังแสดงลักษณะคุณสมบัติรีดอกซ์ขององค์ประกอบ แต่มีความแตกต่างดังต่อไปนี้
อิเล็กโทรเนกาติวิตีให้ลักษณะขององค์ประกอบเดียว ด้วยตัวมันเองนอกเหนือจากการพบในองค์ประกอบของสารประกอบทางเคมีใด ๆ ในขณะที่สถานะออกซิเดชั่นแสดงถึงความสามารถในการลดออกซิเดชั่นเมื่อองค์ประกอบเป็นส่วนหนึ่งของโมเลกุลใด ๆ
เรามาพูดถึงความสามารถในการออกซิไดซ์และความสามารถในการฟื้นฟูคืออะไร
ออกซิเดชัน เป็นกระบวนการถ่ายโอนโฟตอนอิสระ (อิเล็กตรอน) ไปยังองค์ประกอบอื่น การออกซิเดชั่นไม่ได้เป็นการกำจัดอิเล็กตรอนอย่างที่เชื่อกันในทางวิทยาศาสตร์ ... เมื่อองค์ประกอบออกซิไดซ์องค์ประกอบอื่นจะทำหน้าที่เหมือนกรดหรือออกซิเจน (จึงเรียกว่า "ออกซิเดชัน") ในการออกซิไดซ์หมายถึงการทำลายการสลายตัวการเผาไหม้ขององค์ประกอบ ... ความสามารถในการออกซิไดซ์คือความสามารถในการทำให้โมเลกุลถูกทำลายโดยพลังงานที่ถ่ายโอนไปยังพวกมัน (โฟตอนอิสระ) จำไว้ว่าพลังงานทำลายสสารเสมอ
มันน่าทึ่งมากที่มีความขัดแย้งในตรรกะทางวิทยาศาสตร์ที่ไม่มีใครสังเกตเห็นมานานแล้ว
ตัวอย่างเช่น“ ตอนนี้เรารู้แล้วว่าสารออกซิไดซ์คือสารที่ได้รับอิเล็กตรอนและตัวรีดิวซ์คือสารที่ทำให้พวกมันออกไป” (สารานุกรมของนักเคมีรุ่นใหม่บทความ“ ปฏิกิริยารีดอกซ์)”
และตรงนั้นสองย่อหน้าด้านล่าง: "สารออกซิแดนท์ที่แรงที่สุดคือกระแสไฟฟ้า (การไหลของอิเล็กตรอนที่มีประจุลบ)" (อ้างแล้ว)
เหล่านั้น. คำพูดแรกกล่าวว่าสารออกซิแดนท์คือสิ่งที่รับอิเล็กตรอนและตัวที่สองคือสารออกซิแดนท์ที่ยอมแพ้
และข้อสรุปที่ผิดพลาดขัดแย้งกันเช่นนี้ทำให้คุณท่องจำในโรงเรียนและสถาบัน!
เป็นที่ทราบกันดีว่าสารออกซิไดซ์ที่ดีที่สุดคืออโลหะ ยิ่งไปกว่านั้นยิ่งเลขคาบขนาดเล็กและเลขกลุ่มยิ่งใหญ่คุณสมบัติของตัวออกซิไดซ์ก็ยิ่งเด่นชัดมากขึ้น เรื่องนี้ไม่น่าแปลกใจ เราได้พูดถึงสาเหตุของสิ่งนี้ในบทความเกี่ยวกับการวิเคราะห์ตารางธาตุในส่วนที่สองซึ่งเราได้พูดถึงสีของนิวคลีออน จากกลุ่มที่ 1 ถึง 8 สีของนิวคลีออนในองค์ประกอบจะค่อยๆเปลี่ยนจากสีม่วงเป็นสีแดง (ถ้าเราคำนึงถึงสีฟ้าขององค์ประกอบ d และ f ด้วย) การรวมกันของอนุภาคสีเหลืองและสีแดงช่วยในการปลดปล่อยโฟตอนอิสระที่สะสมไว้ สีเหลืองสะสม แต่ยังคงอ่อนแอ และสีแดงมีส่วนทำให้เกิดผลกระทบ การให้โฟตอนคือกระบวนการออกซิเดชั่น แต่เมื่อบางส่วนเป็นสีแดงแสดงว่าไม่มีอนุภาคใดที่สามารถสะสมโฟตอนได้ นั่นคือเหตุผลที่องค์ประกอบของกลุ่มที่ 8 ซึ่งเป็นก๊าซมีตระกูลไม่ใช่ตัวออกซิไดซ์ซึ่งแตกต่างจากฮาโลเจนเพื่อนบ้าน
การกู้คืน เป็นกระบวนการที่ตรงกันข้ามกับการเกิดออกซิเดชัน ปัจจุบันในทางวิทยาศาสตร์เชื่อว่าเมื่อองค์ประกอบทางเคมีได้รับอิเล็กตรอนจะลดลง มุมมองนี้ค่อนข้างเข้าใจ (แต่ไม่เป็นที่ยอมรับ) เมื่อศึกษาโครงสร้างขององค์ประกอบทางเคมีพบว่าปล่อยอิเล็กตรอนออกมา พวกเขาสรุปว่าอิเล็กตรอนเป็นส่วนหนึ่งขององค์ประกอบ ซึ่งหมายความว่าการถ่ายโอนอิเล็กตรอนไปยังองค์ประกอบเป็นการฟื้นฟูโครงสร้างที่สูญหายไป
อย่างไรก็ตามในความเป็นจริงไม่เป็นเช่นนั้น
อิเล็กตรอนเป็นโฟตอนอิสระ พวกเขาไม่ใช่นิวคลีออน พวกเขาไม่ได้เป็นส่วนหนึ่งของร่างกายขององค์ประกอบ พวกมันถูกดึงดูดมาจากภายนอกและสะสมบนพื้นผิวของนิวคลีออนและระหว่างพวกมัน แต่การสะสมของพวกมันไม่ได้นำไปสู่การฟื้นฟูโครงสร้างขององค์ประกอบหรือโมเลกุลเลย ในทางตรงกันข้ามโฟตอนเหล่านี้ปล่อยออกมาโดยอีเธอร์ (พลังงาน) ของพวกมันทำให้อ่อนแอลงและทำลายพันธะระหว่างองค์ประกอบต่างๆ และนี่คือกระบวนการออกซิเดชั่น แต่ไม่ใช่การลดลง
ในการเรียกคืนโมเลกุลในความเป็นจริงคือการใช้พลังงานจากมัน (ในกรณีนี้คือโฟตอนอิสระ) และไม่สื่อสารกับมัน ด้วยการรับโฟตอนองค์ประกอบรีดิวซ์จะควบแน่นสาร - คืนค่า
สารรีดิวซ์ที่ดีที่สุดคือโลหะ คุณสมบัตินี้ตามธรรมชาติมาจากองค์ประกอบเชิงคุณภาพและเชิงปริมาณ - Fields of Attraction มีขนาดใหญ่ที่สุดและมีอนุภาคจำนวนมากหรือเพียงพอบนพื้นผิวเสมอ ของสีฟ้า.
คุณสามารถอนุมานคำจำกัดความของโลหะต่อไปนี้ได้
โลหะ เป็นองค์ประกอบทางเคมีซึ่งชั้นผิวจะต้องมีอนุภาคสีน้ำเงิน
และ ที่ไม่ใช่โลหะ - นี่คือองค์ประกอบในองค์ประกอบของชั้นผิวที่ไม่มีหรือแทบจะไม่มีโฟตอนสีน้ำเงินและมักจะมีสีแดง
โลหะที่มีแรงดึงดูดสูงจะแย่งอิเล็กตรอนออกไปได้อย่างสมบูรณ์แบบ ดังนั้นพวกเขาจึงเป็นผู้บูรณะ
ให้คำจำกัดความของแนวคิด "อิเล็กโตรเนกาติวิตี" "สถานะออกซิเดชั่น" "ปฏิกิริยารีดอกซ์" ซึ่งสามารถพบได้ในตำราเกี่ยวกับเคมี
« สถานะออกซิเดชั่น - ประจุตามเงื่อนไขของอะตอมในสารประกอบซึ่งคำนวณจากสมมติฐานว่าประกอบด้วยไอออนเท่านั้น เมื่อกำหนดแนวความคิดนี้สันนิษฐานตามอัตภาพว่าอิเล็กตรอนที่มีพันธะ (เวเลนซ์) จะถูกถ่ายโอนไปยังอะตอมของอิเล็กโทรเนกาติวิตีมากขึ้นดังนั้นสารประกอบจึงประกอบด้วยไอออนที่มีประจุบวกและลบเช่นเดียวกับที่เป็นอยู่ สถานะออกซิเดชั่นอาจเป็นศูนย์ลบหรือบวกซึ่งโดยปกติจะวางไว้เหนือสัญลักษณ์องค์ประกอบที่ด้านบน
ค่าศูนย์ของสถานะออกซิเดชันเป็นผลมาจากอะตอมของธาตุที่อยู่ในสถานะอิสระ ... ค่าลบของสถานะออกซิเดชั่นมีอะตอมเหล่านั้นซึ่งเมฆอิเล็กตรอนพันธะ (คู่อิเล็กตรอน) ถูกแทนที่ สำหรับฟลูออรีนในสารประกอบทั้งหมดคือ -1 อะตอมที่บริจาคเวเลนซ์อิเล็กตรอนให้กับอะตอมอื่นมีสถานะออกซิเดชันเป็นบวก ตัวอย่างเช่นสำหรับโลหะอัลคาไลและอัลคาไลน์เอิร์ ธ จะมีค่า +1 และ +2 ตามลำดับ ในอิออนอย่างง่ายจะเท่ากับประจุของไอออน ในสารประกอบส่วนใหญ่สถานะออกซิเดชั่นของอะตอมของไฮโดรเจนคือ + 1 แต่ในโลหะไฮไดรด์ (สารประกอบที่มีไฮโดรเจน) และอื่น ๆ จะเป็น –1 สำหรับออกซิเจนสถานะออกซิเดชันคือ -2 แต่ตัวอย่างเช่นเมื่อใช้ร่วมกับฟลูออรีนจะเป็น +2 และในสารประกอบเปอร์ออกไซด์ -1 ...
ผลรวมพีชคณิตของสถานะออกซิเดชันของอะตอมในสารประกอบเป็นศูนย์และในไอออนเชิงซ้อนประจุของไอออน ...
สถานะออกซิเดชั่นสูงสุดคือค่าบวกสูงสุด สำหรับองค์ประกอบส่วนใหญ่จะมีค่าเท่ากับเลขหมู่ในระบบคาบและเป็นลักษณะเชิงปริมาณที่สำคัญขององค์ประกอบในสารประกอบ ค่าที่น้อยที่สุดของสถานะออกซิเดชันขององค์ประกอบซึ่งเกิดขึ้นในสารประกอบมักเรียกว่าสถานะออกซิเดชันต่ำสุด ส่วนที่เหลือทั้งหมดอยู่ในระดับกลาง” (พจนานุกรมสารานุกรมของนักเคมีรุ่นเยาว์บทความ“ สถานะออกซิเดชั่น”)
นี่คือข้อมูลพื้นฐานเกี่ยวกับแนวคิดนี้ มีความเกี่ยวข้องอย่างใกล้ชิดกับอีกคำหนึ่งคืออิเล็กโทรเนกาติวิตี
« อิเล็กโทรเนกาติวิตี - นี่คือความสามารถของอะตอมในโมเลกุลในการดึงดูดอิเล็กตรอนที่เกี่ยวข้องกับการก่อตัวของพันธะเคมี "(พจนานุกรมสารานุกรมของนักเคมีรุ่นใหม่บทความ" อิเล็กโทรเนกาติวิตี ")
“ ปฏิกิริยารีดอกซ์เกิดขึ้นพร้อมกับการเปลี่ยนแปลงสถานะออกซิเดชั่นของอะตอมที่ประกอบเป็นสารตั้งต้นอันเป็นผลมาจากการเคลื่อนที่ของอิเล็กตรอนจากอะตอมของสารรีเอเจนต์ตัวใดตัวหนึ่ง (ตัวรีดิวซ์) ไปยังอะตอมของอีกอะตอม ปฏิกิริยาออกซิเดชั่น - รีดิวซ์พร้อมกันจะเกิดปฏิกิริยาออกซิเดชั่น (การปลดปล่อยอิเล็กตรอน) และการรีดักชัน (การเพิ่มอิเล็กตรอน) "(พจนานุกรมสารานุกรมเคมี, เอ็ดโดย IL Knunyants บทความ" ปฏิกิริยารีดอกซ์ ")
ในความคิดของเรามีข้อผิดพลาดมากมายที่ซ่อนอยู่ในแนวคิดทั้งสามนี้
ในตอนแรก เราเชื่อว่าการก่อตัวของพันธะเคมีระหว่างธาตุทั้งสองไม่ได้เป็นกระบวนการในการเข้าสังคมของอิเล็กตรอน พันธะเคมีคือพันธะแรงโน้มถ่วง อิเล็กตรอนซึ่งคาดว่าจะบินรอบนิวเคลียสเป็นโฟตอนอิสระที่สะสมอยู่บนพื้นผิวของนิวคลีออนภายในร่างกายขององค์ประกอบและระหว่างพวกมัน เพื่อให้การเชื่อมต่อเกิดขึ้นระหว่างสององค์ประกอบโฟตอนอิสระของพวกเขาไม่จำเป็นต้องซ้อนระหว่างองค์ประกอบ สิ่งนี้ไม่เกิดขึ้น ในความเป็นจริงองค์ประกอบที่หนักกว่าจะขจัด (ดึงดูด) โฟตอนอิสระจากโฟตอนที่เบากว่าและเก็บไว้ (อย่างแม่นยำมากขึ้นในตัวมันเอง) และโซนขององค์ประกอบที่เบากว่าซึ่งโฟตอนเหล่านี้ถูกกำจัดออกไปจะกลายเป็นเปลือยมากขึ้นหรือน้อยลง เพราะสิ่งที่ดึงดูดในโซนนี้จึงเป็นที่ประจักษ์ในระดับที่มากขึ้น และองค์ประกอบที่เบากว่าจะดึงดูดไปยังองค์ประกอบที่หนักกว่า นี่คือพันธะเคมีที่เกิดขึ้น
ประการที่สอง เคมีสมัยใหม่มองเห็นความสามารถขององค์ประกอบในการดึงดูดอิเล็กตรอนให้ตัวเองบิดเบี้ยว - กลับหัว เชื่อกันว่ายิ่งอิเล็กโตรเนกาติวิตีขององค์ประกอบมีมากเท่าไหร่ก็จะสามารถดึงดูดอิเล็กตรอนเข้ามาหาตัวเองได้มากขึ้นเท่านั้น ฟลูออรีนและออกซิเจนควรจะทำได้ดีที่สุด - พวกมันดึงดูดอิเล็กตรอนของคนอื่น เช่นเดียวกับองค์ประกอบอื่น ๆ ของ 6 และ 7 กลุ่ม
ความจริงแล้วความคิดเห็นนี้ไม่ใช่อะไรมากไปกว่าความหลงผิด ขึ้นอยู่กับความเข้าใจผิดที่ว่ายิ่งจำนวนกลุ่มมากองค์ประกอบก็จะยิ่งหนัก และยิ่งประจุบวกของนิวเคลียสมีมากขึ้น นี่เป็นเรื่องไร้สาระ นักวิทยาศาสตร์ยังคงไม่ได้เอะใจที่จะอธิบายว่าอะไรที่ถือเป็น "ประจุ" ในมุมมองของพวกเขา เช่นเดียวกับในเชิงตัวเลขพวกเขานับองค์ประกอบทั้งหมดตามลำดับและวางจำนวนประจุตามจำนวน ธุดงค์ครั้งใหญ่!
นอกจากนี้ยังชัดเจนสำหรับเด็กว่าก๊าซเบากว่าโลหะหนาแน่น ในทางเคมีมีความเชื่อกันอย่างไรว่าก๊าซสามารถดึงดูดอิเล็กตรอนเข้าหาตัวเองได้ดีกว่า?
แน่นอนว่าโลหะที่มีความหนาแน่นสูงจะดึงดูดอิเล็กตรอนได้ดีกว่า
แน่นอนว่านักวิทยาศาสตร์เคมีสามารถใช้คำว่า "อิเล็กโทรเนกาติวิตี" ได้เนื่องจากเป็นเรื่องธรรมดา อย่างไรก็ตามพวกเขาจะต้องเปลี่ยนความหมายเป็นตรงกันข้าม
อิเล็กโทรเนกาติวิตี คือความสามารถขององค์ประกอบทางเคมีในโมเลกุลในการดึงดูดอิเล็กตรอนเข้าหาตัวเอง และโดยธรรมชาติแล้วความสามารถนี้แสดงออกในโลหะได้ดีกว่าในอโลหะ
สำหรับเสาไฟฟ้าในโมเลกุลนั้นแท้จริงแล้ว ขั้วลบ - สิ่งเหล่านี้เป็นองค์ประกอบที่ไม่ใช่โลหะที่บริจาคอิเล็กตรอนโดยมี Fields of Attraction ต่ำกว่า และ บวก - สิ่งเหล่านี้เป็นองค์ประกอบที่มีคุณสมบัติเป็นโลหะที่เด่นชัดกว่าเสมอโดยมีจุดดึงดูดมากมาย
มายิ้มให้กัน
อิเล็กโทรเนกาติวิตี - นี่เป็นอีกหนึ่งความพยายามอีกครั้งในการอธิบายคุณภาพขององค์ประกอบทางเคมีพร้อมกับมวลและประจุที่มีอยู่แล้ว ในกรณีนี้มักจะเป็นเช่นนั้นนักวิทยาศาสตร์จากสาขาวิทยาศาสตร์อื่นในกรณีนี้เคมีราวกับว่าไม่ไว้วางใจเพื่อนนักฟิสิกส์ แต่เป็นเพียงเพราะบุคคลใดก็ตามทำการค้นพบไปตามทางของเขาเองและไม่ใช่แค่สำรวจประสบการณ์ของผู้อื่น .
จึงเกิดขึ้นในครั้งนี้
มวลและประจุไม่ได้ช่วยให้นักเคมีเข้าใจสิ่งที่เกิดขึ้นในอะตอมเมื่อพวกมันมีปฏิสัมพันธ์ซึ่งกันและกันและมีการนำอิเล็กโทรเนกาติวิตีมาใช้ - ความสามารถขององค์ประกอบในการดึงดูดอิเล็กตรอนที่เกี่ยวข้องกับการก่อตัวของพันธะเคมี ควรยอมรับว่าความคิดของแนวคิดนี้วางไว้ค่อนข้างถูกต้อง ด้วยการแก้ไขเพียงอย่างเดียวที่สะท้อนความเป็นจริงในรูปแบบกลับหัว ดังที่เราได้กล่าวไปแล้วว่าควรดึงดูดอิเล็กตรอนไปยังโลหะไม่ใช่โลหะ - เนื่องจากลักษณะเฉพาะของสีของนิวคลีออนพื้นผิว โลหะเป็นสารรีดิวซ์ที่ดีที่สุด อโลหะเป็นตัวออกซิไดซ์ โลหะจะถูกนำออกไปและไม่ได้รับโลหะ โลหะ - หยินไม่ใช่โลหะ - หยาง
ความลึกลับเข้ามาช่วยวิทยาศาสตร์ในเรื่องของการทำความเข้าใจความลับของธรรมชาติ
เกี่ยวกับ สถานะออกซิเดชั่น นี่เป็นความพยายามที่ดีในการทำความเข้าใจว่าการกระจายของอิเล็กตรอนอิสระเกิดขึ้นภายในสารประกอบทางเคมี - โมเลกุลอย่างไร
ถ้าสารประกอบทางเคมีเป็นเนื้อเดียวกันนั่นคือมันง่ายโครงสร้างของมันประกอบด้วยองค์ประกอบประเภทเดียวกันแล้วทุกอย่างถูกต้องแน่นอนสถานะออกซิเดชั่นขององค์ประกอบใด ๆ ในสารประกอบจะเป็นศูนย์ เนื่องจากสารประกอบนี้ไม่มีตัวออกซิไดซ์และไม่มีตัวรีดิวซ์ และทุกรายการมีคุณภาพเท่าเทียมกัน ไม่มีใครแย่งอิเล็กตรอนไปไม่มีใครให้มันไป ไม่ว่าจะเป็นสารที่มีความหนาแน่นสูงของเหลวหรือก๊าซก็ไม่สำคัญ
สถานะออกซิเดชั่นเช่นเดียวกับอิเล็กโทรเนกาติวิตีแสดงให้เห็นถึงคุณภาพขององค์ประกอบทางเคมี - ภายในกรอบขององค์ประกอบทางเคมีเท่านั้น สถานะออกซิเดชั่นมีจุดมุ่งหมายเพื่อเปรียบเทียบคุณภาพขององค์ประกอบทางเคมีในสารประกอบ ในความคิดของเราแนวคิดนี้ดี แต่การนำไปใช้ไม่เป็นที่น่าพอใจอย่างสิ้นเชิง
เรากำลังต่อต้านทฤษฎีและแนวคิดทั้งหมดของโครงสร้างขององค์ประกอบทางเคมีและพันธะระหว่างพวกเขาอย่างเด็ดขาด ถ้าเพียงเพราะจำนวนกลุ่มตามความคิดของเราควรมากกว่า 8 นั่นหมายความว่าระบบทั้งหมดกำลังพังทลาย และไม่เพียงแค่นั้น โดยทั่วไปการนับจำนวนอิเล็กตรอนในอะตอม "บนนิ้ว" นั้นไม่ร้ายแรง แต่อย่างใด
ตามแนวคิดปัจจุบันปรากฎว่าประจุไฟฟ้าทั่วไปที่เล็กที่สุดถูกกำหนดให้กับสารออกซิแดนท์ที่แรงที่สุดฟลูออรีนมีประจุ -1 ในสารประกอบทั้งหมดออกซิเจนอยู่ที่ -2 เกือบทุกที่ และสำหรับโลหะที่มีการใช้งานมาก - อัลคาไลน์และอัลคาไลน์เอิร์ ธ - ประจุเหล่านี้ตามลำดับ +1 และ +2 มันไม่สมเหตุสมผลเลย แม้ว่าเราจะพูดซ้ำ แต่เราเข้าใจรูปแบบทั่วไปตามที่ได้ทำไว้ - ทั้งหมดนี้เพื่อประโยชน์ของ 8 กลุ่มในตารางและ 8 อิเล็กตรอนที่ระดับพลังงานภายนอก
อย่างน้อยที่สุดมูลค่าของประจุไฟฟ้าสำหรับฮาโลเจนและออกซิเจนควรมีค่ามากที่สุดโดยมีเครื่องหมายลบ และในโลหะอัลคาไลและอัลคาไลน์เอิร์ ธ ก็มีขนาดใหญ่เช่นกันโดยมีเครื่องหมายบวกเท่านั้น
ใน สารประกอบทางเคมี มีองค์ประกอบที่บริจาคอิเล็กตรอน - ตัวออกซิไดส์, อโลหะ, ประจุลบและองค์ประกอบที่บริจาคอิเล็กตรอน - ตัวรีดิวซ์, โลหะ, ประจุบวก ด้วยวิธีนี้ในการเปรียบเทียบองค์ประกอบเชื่อมโยงซึ่งกันและกันและพยายามกำหนดสถานะออกซิเดชั่น
อย่างไรก็ตามในการค้นหาด้วยวิธีนี้ในความคิดของเราสถานะออกซิเดชั่นไม่ได้สะท้อนความเป็นจริงอย่างถูกต้อง การเปรียบเทียบค่าอิเล็กโทรเนกาติวิตีขององค์ประกอบในโมเลกุลจะถูกต้องกว่า ท้ายที่สุดแล้วอิเล็กโทรเนกาติวิตีเกือบจะเหมือนกับสถานะออกซิเดชั่น (เป็นลักษณะของคุณภาพเฉพาะองค์ประกอบเดียว)
คุณสามารถใช้มาตราส่วนของอิเล็กโตรเนกาติวิตีและใส่ค่าลงในสูตรสำหรับแต่ละองค์ประกอบได้ จากนั้นจะมองเห็นได้ทันทีว่าองค์ประกอบใดให้อิเล็กตรอนและธาตุใดนำออกไป องค์ประกอบที่มีค่าอิเล็กโทรเนกาติวิตีในสารประกอบมากที่สุด - ขั้วลบ - บริจาคอิเล็กตรอน และคนที่มีอิเล็กโทรเนกาติวิตีน้อยที่สุด - ขั้วบวกจะรับอิเล็กตรอน
ถ้ามีให้พูดว่า 3 หรือ 4 องค์ประกอบในโมเลกุลไม่มีอะไรเปลี่ยนแปลง เรายังใส่ค่าของอิเล็กโทรเนกาติวิตีและเปรียบเทียบ
อย่างไรก็ตามอย่าลืมวาดแบบจำลองโครงสร้างของโมเลกุล อันที่จริงแล้วในสารประกอบใด ๆ หากไม่ใช่เรื่องง่ายนั่นคือไม่มีองค์ประกอบประเภทใดชนิดหนึ่งโลหะและอโลหะมีความสัมพันธ์ซึ่งกันและกันก่อนอื่น โลหะรับอิเล็กตรอนจากอโลหะและจับกับพวกมัน และอิเล็กตรอนของธาตุตั้งแต่ 2 ธาตุขึ้นไปที่มีคุณสมบัติของโลหะที่เด่นชัดกว่าก็สามารถพรากจากองค์ประกอบหนึ่งของอโลหะได้ในเวลาเดียวกัน นี่คือลักษณะของโมเลกุลที่ซับซ้อนและซับซ้อนเกิดขึ้น แต่นี่ไม่ได้หมายความว่าในโมเลกุลดังกล่าวองค์ประกอบของโลหะจะเข้าสู่พันธะที่แข็งแกร่งซึ่งกันและกัน บางทีอาจจะตั้งอยู่คนละฟากกัน ถ้าต่อไปพวกเขาจะติดใจ แต่พันธะที่แข็งแกร่งจะเกิดขึ้นก็ต่อเมื่อองค์ประกอบหนึ่งเป็นโลหะมากกว่าอีกองค์ประกอบหนึ่ง มีความจำเป็นที่องค์ประกอบหนึ่งจะเลือกอิเล็กตรอน - ลบออก มิฉะนั้นองค์ประกอบจะไม่ถูกเปิดเผย - ปลดปล่อยจากโฟตอนอิสระบนพื้นผิว สนามแห่งการดึงดูดจะไม่ปรากฏอย่างสมบูรณ์และจะไม่มีการเชื่อมต่อที่ชัดเจน มัน หัวข้อที่ซับซ้อน - การศึกษา พันธะเคมีและเราจะไม่ลงรายละเอียดเกี่ยวกับเรื่องนี้ในบทความนี้
เราเชื่อว่าเราได้อธิบายรายละเอียดที่เพียงพอเกี่ยวกับหัวข้อที่อุทิศให้กับการวิเคราะห์แนวคิดของ "อิเล็กโตรเนกาติวิตี" "สถานะออกซิเดชั่น" "ออกซิเดชั่น" และ "การลดลง" และให้ข้อมูลที่น่าสนใจมากมายแก่คุณ
จากหนังสือ Guided Dreams ผู้เขียน Mir Elenaการฟื้นฟู“ เมื่อสัญญาณเดียวของความเป็นปัจเจกเกิดขึ้นสาระสำคัญและชีวิตจะถูกแบ่งออกเป็นสองส่วน นับจากนี้ไปเว้นแต่สันติภาพสุดท้ายจะถึงจุดสำคัญและชีวิตจะไม่ได้พบกันอีกต่อไป " วิลเลียม "ความลับของดอกไม้สีทอง" หลังเลิกเรียน
จากหนังสือ The Book of Secrets สิ่งที่ชัดเจนอย่างไม่น่าเชื่อบนโลกและที่อื่น ๆ ผู้เขียน Vyatkin Arkady Dmitrievichมาโซคิสม์เป็นระดับที่รุนแรงของการดูดเลือดโดยสมัครใจในแง่นี้มาโซคิสม์คล้ายกับการพึ่งพาอาศัยกัน มาโซคิสต์คือคนที่ได้รับความรู้สึกที่น่าพอใจจากความทุกข์ทรมานทางร่างกายและจิตใจของตนเอง กล่าวอีกนัยหนึ่งคือพวกชอบทุบตีดุรังแก
จากหนังสือแวมไพร์ในรัสเซีย ทุกสิ่งที่คุณต้องการรู้เกี่ยวกับพวกเขา! ผู้เขียน บาวเออร์อเล็กซานเดอร์วิธีกำหนดระดับการสูญเสียเลือดเมื่อแวมไพร์ดื่มเลือดเขาจะดื่มเลือดครั้งละครึ่งลิตรถึงหนึ่งลิตรครึ่ง ร่างกายมนุษย์มีเลือดเพียงห้าถึงหกลิตรดังนั้นการสูญเสียเลือดนี้จึงไม่จำเป็นต้องเป็นอันตรายถึงชีวิต อย่างไรก็ตามแวมไพร์สามารถ
จากหนังสือ Modeling the Future in a Dream ผู้เขียน Mir Elenaการฟื้นตัวหลังจากสำเร็จการศึกษาทำงานเป็นวิศวกรในองค์กรปิดฉันตระหนักว่าฉันไม่ได้อยู่ในสถานที่ของฉันดังนั้นฉันจึงตัดสินใจเปลี่ยนอาชีพและเข้าโรงเรียนดนตรีแจ๊สแห่งการด้นสดและต่อมาแผนกคลาสสิกของโรงเรียนดนตรี
จากหนังสือกฎทองของฮวงจุ้ย 10 ขั้นตอนง่ายๆสู่ความสำเร็จความเป็นอยู่และอายุที่ยืนยาว ผู้เขียน Ogudin Valentin Leonidovichระดับอิทธิพลเชิงลบของวัตถุภายนอกวัตถุภายนอกมีอิทธิพลเชิงลบมากที่สุดโดยอยู่ด้านหน้าทางเข้าบ้านโดยตรง แต่ยิ่งตั้งอยู่ในมุมของทางเข้ามากเท่าไหร่อิทธิพลของพวกเขาก็จะยิ่งอ่อนแอลงเท่านั้น
ผู้เขียน Shure Eduardระดับแรก: การทำอาหาร งานเทศนาบนภูเขาและอาณาจักรของพระเจ้าพระคริสต์เริ่มต้นด้วยไอดีลของชาวกาลิลีและการประกาศเรื่อง "อาณาจักรของพระเจ้า" คำทำนายนี้ชี้ให้เราเห็นถึงคำสอนที่เป็นที่นิยมของเขา ในขณะเดียวกันก็เป็นการเตรียมความพร้อมให้ประเสริฐยิ่งขึ้น
จากหนังสือ Divine Evolution จากสฟิงซ์ถึงพระคริสต์ ผู้เขียน Shure Eduardระดับที่สองของการเริ่มต้น (การทำให้บริสุทธิ์) การรักษาที่น่าอัศจรรย์ การบำบัดของคริสเตียนในความลึกลับโบราณทั้งหมดการเตรียมทางศีลธรรมและทางปัญญาตามมาด้วยการทำให้จิตวิญญาณบริสุทธิ์ซึ่งจะทำให้อวัยวะใหม่ในนั้นฟื้นคืนชีพและต่อมาให้ความสามารถ
จากหนังสือ The Riddle of the Great Sphinx ผู้เขียน Barbaren Georgesการบูรณะรูปปั้นอายุที่แท้จริงของมหาสฟิงซ์ย้อนกลับไปถึงจุดเริ่มต้นของยุคอาดามิก อย่างน้อยเขาก็เป็นคนร่วมสมัยของปิรามิดซึ่งเป็นวงดนตรีที่เขาเห็นแล้วเสร็จด้วยตัวเขาเองภาพของมหาสฟิงซ์ถูกเปิดเผยในหลายศตวรรษที่ผ่านมา
จากหนังสือ Healing the Soul. 100 เทคนิคการทำสมาธิแบบฝึกหัดเพื่อการบำบัดและการผ่อนคลาย ผู้เขียน Rajneesh Bhagwan Shriคืนจังหวะ ... กำหนดเวลาเดิมที่จะเข้านอน - ถ้าทุกเย็นเป็นเวลาสิบเอ็ดโมงก็สิบเอ็ดนี่เป็นครั้งแรกเริ่มเวลาที่แน่นอนและอีกไม่นานร่างกายก็จะเข้าสู่จังหวะนี้ได้ อย่าเปลี่ยนเวลานี้มิฉะนั้นคุณจะสับสนกับร่างกาย ร่างกาย
ผู้เขียน Kuzmishin E.L.การรับปริญญาของเด็กฝึกงานการรับปริญญาฝึกงานการตกแต่งกล่องและเสื้อคลุมผนังและเพดานของกล่องควรแขวนด้วยผ้าสีฟ้าและสีขาวโดยไม่ต้องปิดทอง เหนือศีรษะของพระอาจารย์ที่เคารพบูชามีรูปสามเหลี่ยมล้อมรอบด้วยรัศมีที่มีชื่อจารึกอยู่ตรงกลาง
จากหนังสือ Cagliostro และ Egyptian Freemasonry ผู้เขียน Kuzmishin E.L.การเข้ารับปริญญาของการตกแต่งของเด็กฝึกงานของลอดจ์และเสื้อกั๊กผนังและเพดานของลอดจ์จะแขวนด้วยผ้าสีฟ้าและสีขาวโดยไม่ต้องปิดทอง เหนือศีรษะของพระอาจารย์เป็นรูปสามเหลี่ยมที่ล้อมรอบด้วยรัศมีที่มีชื่อ "พระยะโฮวา" จารึกอยู่ตรงกลางปัก
จากหนังสืออัตชีวประวัติของโยคี ผู้เขียน โยกานันดาพาราหรรษาบทที่ 23 ฉันกำลังได้รับปริญญาจากมหาวิทยาลัย - คุณไม่สนใจคำจำกัดความทางปรัชญาในตำราของคุณไม่ต้องสงสัยเลยว่าการใช้ "สัญชาตญาณ" ที่ไม่สร้างความรำคาญเพื่อนำทางคุณไปสู่การสอบ แต่ถ้าคุณไม่เร่งด่วนหันไปใช้วิธีการทางวิทยาศาสตร์มากขึ้นฉันก็ต้องทำ
จากหนังสือคับบาลาห์. โลกบน. จุดเริ่มต้นของวิธีการ ผู้เขียน Laitman Michael7.5. ระดับของจิตสำนึกแห่งความชั่วร้ายตามที่อธิบายไว้ในบทความ“ การให้โตราห์” ความสุขและความสุขนั้นพิจารณาจากระดับความคล้ายคลึงกับผู้สร้างในคุณสมบัติและความทุกข์และความอดทนจะพิจารณาจากระดับความแตกต่างจากผู้สร้าง ดังนั้นความเห็นแก่ตัวจึงน่ารังเกียจสำหรับเราและเจ็บปวดเหลือทน
ตัวเลือกที่ 1
1. ตรวจสอบสถานะออกซิเดชันของอะตอมขององค์ประกอบทางเคมีในสารประกอบต่อไปนี้: HNO₂, NO₂, H₃N, SO₂, N₂O
2. ใช้ตารางธาตุจัดเรียงองค์ประกอบต่อไปนี้ตามลำดับการลดอิเล็กโทรเนกาติวิตี: O, N, Be, B, Li, C. กำหนดตำแหน่งที่ฟลูออรีนและโซเดียมควรอยู่ในแถวนี้ อธิบายคำตอบ 
3. สถานะออกซิเดชันของอะตอมกำมะถันเปลี่ยนไปอย่างไรในระหว่างการเกิดออกซิเดชันของSO₂เป็นSO₃? อธิบายคำตอบ
ทางเลือกที่ 2
1. ตรวจสอบสถานะออกซิเดชันของอะตอมขององค์ประกอบทางเคมีในสารประกอบต่อไปนี้: CO₂, H₃PO₄, SiH₄, P₂O₅, Mg₂Si
2. ในทิศทางของอะตอมที่มีองค์ประกอบทางเคมีร่วมกัน คู่อิเล็กทรอนิกส์, ในโมเลกุลของสารประกอบต่อไปนี้: BF₃, PCl₃, CS₂, CCl₄, HBr? ให้คำตอบที่มีเหตุผล
3. สถานะออกซิเดชันของคาร์บอนเปลี่ยนไปในระหว่างการก่อตัวหรือไม่ กรดคาร์บอนิก H₂CO₃ทำจากคาร์บอนไดออกไซด์และน้ำ? อธิบายคำตอบ
ตัวเลือก 3
1. ตรวจสอบสถานะออกซิเดชันของอะตอมขององค์ประกอบทางเคมีในสารประกอบต่อไปนี้: Cl₂, NaClO, CaCl₂, HF, SO₃, Cl₂O₇
2. การใช้ ระบบธาตุ องค์ประกอบทางเคมีจัดเรียงองค์ประกอบต่อไปนี้ตามลำดับอิเล็กโทรเนกาติวิตีจากน้อยไปมาก: P, Al, Cl, Na, S, Mg หาจุดในแถวนี้สำหรับโพแทสเซียมและฟลูออไรด์ อธิบายคำตอบ 
3. สถานะออกซิเดชันของคาร์บอนเปลี่ยนไปอย่างไรเมื่อเผาไหม้มีเธน CH метด้วยการก่อตัวของคาร์บอนมอนอกไซด์ (IV) และน้ำ? อธิบายคำตอบ
ทางเลือกที่ 4
1. ตรวจสอบสถานะออกซิเดชันของอะตอมขององค์ประกอบทางเคมีในสารประกอบต่อไปนี้: H₂SO₄, SO₂, NO₂, BF₃, H₂S
2. ต่ออะตอมของอะไร องค์ประกอบทางเคมี คู่อิเล็กตรอนทั่วไปจะถูกแทนที่ในโมเลกุลของสารประกอบต่อไปนี้: H₂O, PCl₃, H₃N, H₂S, CO₂? ให้คำตอบที่มีเหตุผล
3. สถานะออกซิเดชันของอะตอมเปลี่ยนไปหรือไม่เมื่อน้ำเกิดจาก สารง่ายๆ - ไฮโดรเจนและออกซิเจน? อธิบายคำตอบ


