Umeme huitwa mali ya kipengele cha kemikali ili kuvutia elektroni kwa atomi yake kutoka kwa atomi za vipengele vingine ambavyo kipengele hiki hufanya dhamana ya kemikali katika uhusiano.
Wakati dhamana ya kemikali imeundwa kati ya atomi ya vipengele tofauti, wingu la umeme la umeme kwa atomi zaidi ya electrone-hasi, ndiyo sababu uhusiano unakuwa polar polar, na tofauti kubwa ya electronegateness - ion.
Umeme unazingatiwa wakati wa kuandika formula za kemikali: ishara ya kipengele cha electronegative kinarekodi katika uhusiano wa binary.
Umeme huongezeka kwa mwelekeo kutoka kushoto kwenda kulia kwa vipengele vya kila kipindi na hupungua kwa mwelekeo kutoka juu hadi chini kwa vipengele vya kundi moja la PS.
Valence. Kipengele kinachoitwa mali ya atomi zake kushikamana na idadi fulani ya atomi nyingine.
Kuna stoichiometric, valence elektroniki na idadi ya uratibu. Tutazingatia tu valence stoichiometric.
Stoichiometric. Valence inaonyesha jinsi atomi ngapi za kipengele kingine huhusisha atomi ya kipengele hiki. Kwa kila kitengo cha valence ilipitishwa valence ya hidrojeni, kwa sababu Hydrogeni daima ni monovalent. Kwa mfano, katika HCl, h 2 o, nH 3 misombo (maandishi sahihi ya amonia h 3 n tayari kutumika katika miongozo ya kisasa), Ch 4 klorini ni monovalent, oksijeni bivalent, nitrojeni na kaboni tetravalenten.
Valence ya stoichiometric ya oksijeni ni kawaida sawa na 2. Kwa kuwa karibu vipengele vyote hufanya misombo na oksijeni, ni rahisi kutumia kama kumbukumbu ya kuamua valence ya kipengele kingine. Kwa mfano, katika misombo na 2 o, COO, FE 2 O 3, hivyo 3 sodiamu monovalent, cobalt bivalent, chuma ni trivalent, sulfuri hexavalent.
Katika athari za vioksidishaji na marekebisho, itakuwa muhimu kwetu kuamua digrii za vipengele vya oxidation.
Shahada ya oxidation. Kipengele katika dutu hii inaitwa valence yake ya stoichiometric, iliyochukuliwa na ishara ya pamoja au chini.
Vipengele vya kemikali vinagawanywa katika vipengele. valence ya kudumu Vipengele vya valence variable.
1.3.3. Vitu vya molekuli na zisizo za elastic. Aina ya lattice ya kioo. Utegemezi wa mali ya vitu kutoka kwa muundo na muundo wao.
Kulingana na hali gani ya kiwanja ni katika asili, imegawanywa katika Masi na isiyo ya kawaida. In. vitu vya molekuli. Chembe ndogo za miundo ni molekuli. Dutu hizi zina lattice ya kioo ya molekuli. Katika vitu visivyo vya mecular, atomi au ions ni chembe ndogo za miundo. Sauti ya kioo ni atomiki, ion au chuma.
Aina ya lattice ya kioo kwa kiasi kikubwa huamua mali ya vitu. Kwa mfano, metali ya kuwa nayo aina ya chuma ya crystal lattice.tofauti na mambo mengine yote. prifiki ya juu, conductivity ya umeme na mafuta. Mali hizi, pamoja na wengine wengi - Kuunda, chuma gloss, nk. Kutokana na aina maalum ya mawasiliano kati ya atomi za chuma - uunganisho wa chuma. Ikumbukwe kwamba mali zinazohusika katika metali zinaonyeshwa tu katika hali iliyopunguzwa. Kwa mfano, fedha katika hali ya gesi haina mali ya kimwili ya metali.
Aina maalum ya mawasiliano katika metali ni metali - kutokana na upungufu wa elektroni valence, hivyo ni kawaida kwa muundo mzima wa chuma. Mfano rahisi zaidi wa muundo wa chuma ulidhani kuwa latti ya kioo ya madini ina ions chanya iliyozungukwa na elektroni za bure, harakati za elektroni hutokea machafuko, kama molekuli ya gesi. Hata hivyo, mfano huo, kuelezea sifa nyingi za metali, na hundi ya kiasi hugeuka kuwa haitoshi. Maendeleo zaidi ya nadharia ya hali ya chuma imesababisha uumbaji nadharia ya eneo la metaliambayo inategemea maonyesho ya mechanics ya quantum.
Katika nodes ya latti ya kioo kuna cations na atomi za chuma, na elektroni huhamia kwa uhuru kwenye safu ya kioo.
Mali ya mitambo ya metali ni plastikiKutokana na upekee wa muundo wa ndani wa fuwele zao. Chini ya plastiki, uwezo wa miili chini ya hatua ya majeshi ya nje ya kufanyiwa deformation, ambayo bado na baada ya kukomesha ushawishi wa nje. Mali hii ya metali inaruhusu kuwapa fomu tofauti wakati wa kukata, wapanda chuma kwenye karatasi au kuivuta kwenye waya.
Plastiki ya metali ni kutokana na ukweli kwamba kwa madhara ya nje ya tabaka ya ions kutengeneza latti ya kioo, kubadilishwa jamaa kwa kila mmoja bila kuvunja. Hii hutokea kwa sababu ya ukweli kwamba kuhamia elektroni kutokana na ugawaji wa bure unaendelea kuwasiliana kati ya tabaka ya ion. Katika athari ya mitambo juu ya imara na grille ya nyuklia, tabaka zake tofauti ni kubadilishwa na kujitoa kati yao ni kuvunjwa kutokana na kupasuka mahusiano mazuri.
ions.Kisha vitu hivi vinafanya aina ya ion ya crystal.

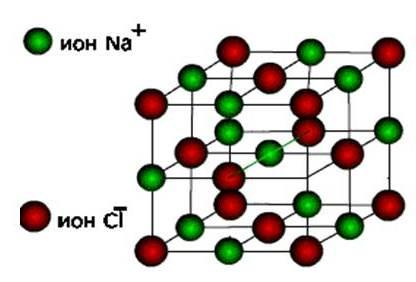
Hizi ni chumvi, pamoja na oksidi na hidrojeni ya metali ya kawaida. Hizi ni vitu imara, tete, lakini ubora wao kuu : Ufumbuzi na kutengeneza misombo hii hufanya sasa umeme.
Ikiwa katika nodes ya latti ya kioo iko aTOMS.Kisha vitu hivi vinafanya aina ya Atomic ya Crystal Lattice.(Diamond, Bor, alumini ya silicon na oksidi za silicon). Kwa mujibu wa mali, imara sana na ya kukataa, isiyo na maji.
Ikiwa katika nodes ya latti ya kioo iko molekuliFomu hizi (chini ya hali ya kawaida ya gesi na vinywaji: o 2, HCl; i 2 dutu za kikaboni.).
Ni jambo la kushangaza kutambua chuma cha gallium, ambacho hutengana na joto la 30 o C. Anomaly hii inaelezwa na ukweli kwamba GA 2 molekuli na mali zake ziko katika makanisa ya bandia ya kioo.
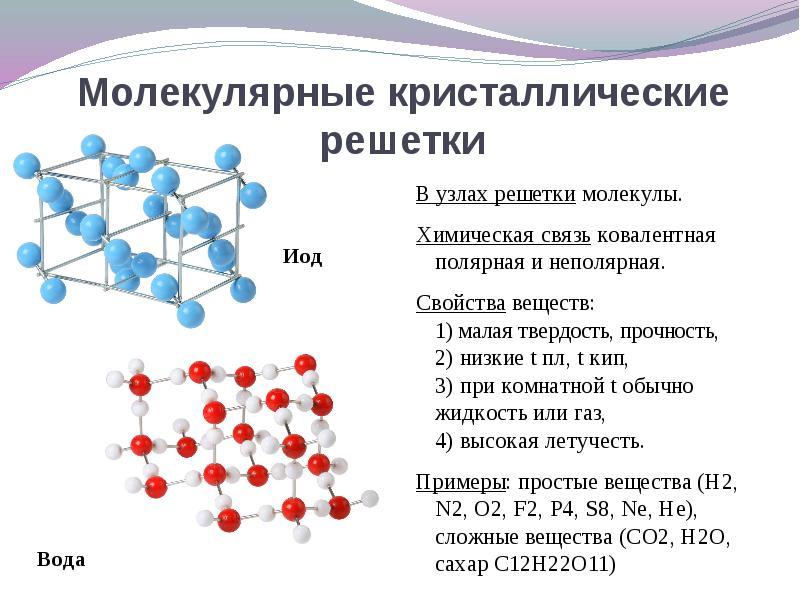
Mfano.Mfumo wa Nemolecular una wote wasio na metali ya kikundi:
1) kaboni, boron, silicon; 2) fluorine, bromine, iodini;
3) oksijeni, sulfuri, nitrojeni; 4) chlorini, fosforasi, seleniamu.
In. dutu zisizo za elastic. Chembe ndogo za miundo ni atomi au ions. Kiti cha kioo ni atomiki, ionic au chuma.
Kwa suluhisho Swali hili ni rahisi kwenda kutoka kinyume. Ikiwa katika nodes ya latti ya kioo iko molekuliKisha vitu hivi vinafanya aina ya Masi ya Crystal Lattice.(Chini ya hali ya kawaida ya gesi na vinywaji: o 2, HCl; pia i 2, sauti ya sauti ya phosphorus p 4, vitu vya kikaboni). Kwa mali, hizi ni misombo ya chini ya kuyeyuka.
Katika jibu la pili kuna gesi ya fluorine, katika gesi ya tatu ya oksijeni, nitrojeni, katika gesi ya nne ya klorini. Hivyo vitu hivi vina lattice ya kioo ya molekuli na muundo wa molekuli.
In. kwanza Jibu vitu vyote - misombo imara chini ya hali ya kawaida na kuunda grille ya nyuklia, ambayo ina maana kwamba kuna maadili yasiyo ya maadili.
Jibu sahihi:1) carbon, Bor, silicon.
- Electronegative mdogo ni kipengele cha kemikali.
- iron.
- magnesiamu.
- kalsiamu.
Tahadhari inapaswa kulipwa kwa maneno "angalau electronegative", i.e. kipengele na mali kubwa ya chuma. Majadiliano haya yataondokana na majibu ya azot iwezekanavyo kama yasiyo ya metall, na kukaa kwenye kalsiamu, kama kazi nyingi za metali zilizopendekezwa katika kazi hiyo. Jibu: 4.
- Bond ya kemikali ya polar katika moja ya molekuli
- Cl 4.
- St. 4.
Maarifa ya mifumo ya mabadiliko katika electron monateness katika vipindi na makundi ya mfumo wa mara kwa mara Di Mendeleev inafanya uwezekano wa kuwatenga kutoka kwenye orodha ya misombo ya quadricular ya carbon methane ch 4, na kutoka kwa halides iliyobaki kuacha CF 4, kama ilivyo kiwanja cha kaboni na electronegative zaidi ya vipengele vyote vya kemikali - fluorine. Jibu: 2.
- Katika molekuli ya kloridi na mawasiliano ya kemikali ya klorini, kwa mtiririko huo.
- ionic na polar covalent.
- ionic na covalent yasiyo ya polar.
- polar covalent na covalent yasiyo ya polar.
- hidrojeni na covalent yasiyo ya polar.
Neno la msingi la utekelezaji wa haraka na sahihi wa kazi hii ni neno "kwa mtiririko huo". Katika matoleo yaliyopendekezwa, moja tu ya majibu huanza kwa maneno "polar covalent", i.e. vifungo sifa ya chloroodor. Jibu: 3.
- Kiwango cha oxidation ya manganese katika kiwanja, fomu ya 2 MNO 4, ni sawa
Ujuzi wa sheria za kuhesabu digrii za oxidation ya vipengele na formula itawawezesha kuchagua jibu sahihi. Jibu: 3.
- Kiwango kidogo cha oxidation kina sulfuri katika chumvi
- sulfate potassium.
- sulfit potasiamu.
- sulfide potasiamu.
- hydrosulfate ya potasiamu.
Kwa wazi, utimilifu wa haraka wa kazi hii utakuwa kutafsiri majina ya chumvi katika formula. Tangu sulfuri ni kipengele cha kikundi kupitia, basi kiwango chake cha chini cha oxidation ni -2. Thamani hii inafanana na kiwanja na formula k 2 - sulfide ya potasiamu. Jibu: 3.
- Kiwango cha oxidation ni atomi +5 ya klorini ina katika ion
- C1O - 4.
- C1O -
- C1O - 3.
- C1O - 2.
Wakati wa kufanya kazi hii, unapaswa kuzingatia ukweli kwamba hakuna misombo ya elektroniki katika hali hiyo, lakini ions ya klorini na malipo moja hasi ("-"). Kwa kuwa jumla ya digrii ya oxidation ya atomi katika ion ni sawa na malipo ya ion, jumla ya malipo hasi ya atomi za oksijeni katika ion iliyoelezwa lazima iwe -6 (+5 - 6 \u003d -1). Jibu: 3.
- Kiwango cha oxidation -3 nitrojeni ina katika kila moja ya uhusiano mawili
- NF 3 na NH 3.
- Nh 4 cl na n 2 o 3.
- Nh 4 cl na nh 3.
- HNO 2 na NF 3.
Kuamua jibu sahihi, ni muhimu kugawanya chaguzi kwa majibu kwa beep ya kushoto na kulia. Kisha chagua moja ambayo misombo ina muundo rahisi - kwa upande wetu, hii ni kiwanja cha binary cha kulia. Uchunguzi utaondoa majibu ya 2 na 4, kama katika oksidi na fluoride katika nitrojeni kiwango cha chanya cha oxidation, kama katika kipengele cha chini cha electronegative. Majadiliano haya yanawezekana kuwatenga na kujibu 1, kwani ni dutu ya kwanza - yote ya nitrojeni fluoride. Jibu: 3.
- Kwa dutu za muundo wa Masi hazijumuishi
- dioksidi ya kaboni.
- methane.
- chloroorod.
- calcium carbonate.
Unapaswa kuzingatia hukumu mbaya, imewekwa katika hali ya kazi. Kwa kuwa vitu vyenye gesi chini ya hali ya kawaida vina grille ya fuwele ya molekuli katika hali imara, hali ya kazi 1-3 haifai na hali ya hali. Calcium Carbonate Attribution kwa chumvi tena inathibitisha jibu sahihi. Jibu: 4.
- Je, hukumu zifuatazo kuhusu mali za vitu na muundo wao?
A. Nguo ya mvua hukaa baridi kwa sababu vitu vya muundo wa molekuli vina uwezo wa upungufu (sublimation).
B. Nguo za mvua hukaa baridi kwa sababu molekuli za maji zina uzito mdogo wa Masi.
- kweli tu A.
- haki tu B.
- hukumu zote mbili ni kweli.
- hukumu zote sio kweli.
Maarifa mali ya kimwili Dutu za muundo wa Masi hufanya iwezekanavyo kuamua kuwa sababu ya kukausha kavu kavu katika baridi ni uwezo wa barafu kwa upungufu, na sio muundo wa dipole wa molekuli ya maji. Jibu: 1.
- Mfumo wa Masi una kila kitu, kanuni ambazo zinapewa mfululizo
- CO 2, HNO 3, SAO.
- NA 2 S, BR 2, NO 2.
- H 2 SO 4, CU, O 3.
- SO 2, I 2, NSL.
Kwa kuwa chaguo zilizopendekezwa zina vitu vitatu, ni mantiki kugawanya matoleo haya katika beeps tatu za wima. Uchunguzi wa kila mmoja wao, kuanzia na vitu vya utungaji rahisi (wastani wa podstolbik), itaondoa majibu ya 3, kwa kuwa ina shaba ya chuma, kuwa na gridi ya kioo ya chuma. Uchambuzi sawa wa beep sahihi utafanya iwezekanavyo kuondokana na majibu ya 1, kwa kuwa ina oksidi ya chuma cha lami (lattice ya ion). Kati ya chaguzi mbili zilizobaki, ni muhimu kuondokana na chaguo 2, kwa kuwa ina chumvi ya chuma ya alkali - sulfidi ya sodiamu (lattice ya ion). Jibu: 4.
Kazi kwa kazi ya kujitegemea.
- Kiwango cha oxidation ni maonyesho + ya nitrojeni katika kiwanja, formula ambayo
- N 2 O 5.
- N 2 O 4.
- N 2 O.
- Kiwango cha oxidation ya chromium katika kiwanja, formula ambayo (NH 4) 2 CR 2 O 7, ni sawa na
- Kiwango cha oxidation ya nitrojeni hupungua kwa safu ya vitu, kanuni ambazo
- NH 3, NO 2, KNO 3.
- N 2 o 4, kno 2, nh 4 cl
- N 2, n 2 o, nh 3.
- HNO 3, HNO 2, NO 2.
- Kiwango cha oxidation ya klorini huongezeka kwa idadi ya vitu, formula
- NSLO, NSLO 4, KSLO 3.
- Cl 2, C1 2 O 7, KSLO 3
- CA (C1O) 2, KSLO 3, NSLO 4
- KSL, KSLO 3, KSLO.
- Mawasiliano ya kemikali ya polar katika molekuli.
- amonia
- serovodorod.
- bromodorod.
- fluorodorod.
- Dutu na dhamana isiyo ya polar ya polar.
- phosphorus nyeupe.
- alumini Phosphide.
- kloridi ya phosphorus (V)
- phosphate ya kalsiamu
- Formula ya vitu tu na dhamana ya ion iliyoandikwa mfululizo
- kloridi ya sodiamu, kloridi ya phosphorus (V), phosphate ya sodiamu
- oxydi ya sodiamu, hidroksidi ya sodiamu, peroxide ya sodiamu.
- seroublerod, caldium carbide, oksidi ya kalsiamu
- calcium fluoride, oksidi ya kalsiamu, kloridi ya kalsiamu.
- Atomic Crystal Lattice ina
- oksidi ya sodiamu.
- oksidi ya kalsiamu
- oksidi ya sulfuri (iv)
- alumini oksidi
- Uhusiano na ionic. crystal Lattice. sumu wakati klorini inavyohusiana na
- fosforasi
- barium.
- hydrogen.
- kijivu
- Je, hukumu zifuatazo kuhusu kloridi ya amonia?
A. kloridi ya ammoniamu ni dutu ya muundo wa ionic iliyoundwa na mahusiano ya polar na ya ionic.
B. Chloride ya Ammoniamu - Dutu ya muundo wa ion, na hivyo imara, refractory na yasiyo ya tete.
- kweli tu A.
- haki tu B.
- hukumu zote mbili ni kweli.
- hukumu zote mbili si sahihi.
08. Umeme, shahada ya oxidation, oxidation na kupona.
Hebu tuzungumze maana ya dhana zinazovutia sana ambazo zipo katika kemia, na mara nyingi hutokea katika sayansi, kwa kutosha kuchanganya, na kutumika katika fomu iliyoingizwa. Itakuwa juu ya "electronegativity", "kiwango cha oxidation" na "athari za redox".
Je! Hii inamaanisha - dhana hutumiwa katika fomu iliyoingizwa?
Tutajaribu kusema hatua kwa hatua kuhusu hilo.
Umeme. Inatuonyesha mali ya redox ya kipengele cha kemikali. Hiyo ni, uwezo wake wa kuchukua au kutoa picha za bure. Na pia ni chanzo au nishati absorber (ether). Yang au Yin.
Shahada ya oxidation. - Hii ni dhana sawa na dhana ya "electronegativity". Pia inaonyesha mali ya redox ya kipengele. Lakini kati yao kuna tofauti ya pili.
Umeme hutoa tabia ya kipengele tofauti. Kwa yenyewe, nje ya kuipata katika kiwanja cha kemikali. Wakati kiwango cha oxidation kinaonyesha uwezo wake wa vioksidishaji na urejesho wakati kipengele ni sehemu ya molekuli yoyote.
Hebu tuzungumze kidogo kuhusu kile ambacho ni uwezo wa oxidize, na ni uwezo gani wa kurejesha.
Oxidation. - Hii ni mchakato wa kuhamisha kwa kipengele kingine cha picha za bure (elektroni). Oxidation haifai elektroni wakati wote, kama ilivyo sasa inaonekana kuwa katika sayansi. . Wakati kipengele kinapunguza kipengele kingine, hufanya kama asidi au oksijeni (kwa hiyo jina "oxidation"). Oxidize - ina maana ya kukuza uharibifu, kuoza, vipengele vya kuchoma . Uwezo wa oxidize ni uwezo wa kusababisha uharibifu wa molekuli na nishati zinazopitishwa na wao (photons huru). Kumbuka kwamba nishati daima huharibu dutu hii.
Kushangaa, kwa muda gani katika sayansi kuna tofauti katika mantiki, haijulikani na mtu yeyote.
Hapa, kwa mfano: "Sasa tunajua kwamba wakala wa oxidizing ni dutu ambayo elektroni hupata, na wakala wa kupunguza ni dutu inayowapa" (encyclopedia ya chemist mdogo, makala "oxidation na mmenyuko)".
Na mara moja, aya mbili hapa chini: "Oxidizer nguvu ni umeme wa sasa (mkondo wa elektroni kushtakiwa)" (ibid.).
Wale. nukuu ya kwanza inasema kuwa wakala wa oxidizing ni nini electrons inachukua, na katika wito wa pili wa kioksidisha kile kinachopa.
Na hitimisho sawa sawa ambayo inapingana na kila mmoja inalazimika kukariri katika shule na taasisi!
Inajulikana kuwa vioksidishaji bora ni yasiyo ya metali. Aidha, idadi ndogo ya idadi na idadi ya kikundi zaidi, nguvu ya mali ya vioksidishaji huelezwa. Hii haishangazi. Tulipoteza sababu za hili katika makala iliyotolewa kwa uchambuzi wa mfumo wa mara kwa mara, katika sehemu ya pili, ambapo walizungumza juu ya rangi ya nucleons. Kutoka kwa kundi la 1 hadi 8, rangi ya vipengele katika vipengele ni hatua kwa hatua kubadilika kutoka kwa zambarau hadi nyekundu (ikiwa unafikiria rangi ya bluu ya D- na F-Elements). Mchanganyiko wa chembe za njano na nyekundu huwezesha kurudi kwa photons za bure zilizokusanywa. Njano hujilimbikiza, lakini kushikilia dhaifu. Na nyekundu huchangia kurudi. Weka photoni - hii ni mchakato wa oxidation. Lakini wakati wengine ni nyekundu, basi hakuna chembe ambazo zinaweza kukusanya photoni. Ndiyo sababu vipengele vya makundi 8, gesi zenye heshima, sio mawakala wa oksidi, tofauti na majirani zao, halogen.
Marejesho - Hii ni mchakato kinyume na oxidation. Sasa, katika sayansi, inaaminika kuwa wakati kipengele cha kemikali kinapata elektroni, ni kurejeshwa. Hatua hii ya mtazamo inawezekana kabisa kuelewa (lakini si kukubali). Wakati wa kusoma muundo wa vipengele vya kemikali, iligunduliwa kuwa hutoa elektroni. Alihitimisha kuwa elektroni ni sehemu ya vipengele. Ina maana kwamba uhamisho wa kipengele cha elektroni ni, aina, marejesho ya muundo wake uliopotea.
Hata hivyo, kwa kweli, kila kitu ni kibaya.
Elektroni ni photoni za bure. Hao ni kiini. Hao sehemu ya mwili wa kipengele. Wanavutiwa na kuingia nje, na kujilimbikiza juu ya uso wa nucleons na kati yao. Lakini mkusanyiko wao sio kabisa kurejesha muundo wa kipengele au molekuli. Kwa upande mwingine, photons hizi zimetolewa na ether (nishati) kudhoofisha na kuharibu viungo kati ya vipengele. Na hii ni mchakato wa oxidation, lakini sio kupona.
Kurejesha molekuli, kwa kweli, - kuchukua nishati kutoka kwake (katika kesi hii, photons bure), na si ripoti. Kuchagua photons, server server compacts dutu - kurejesha.
Wakala bora wa kupunguza ni metali. Mali hii hufuata kutoka kwa utungaji wao wa ubora na kiasi - maeneo yao ya kivutio ni kubwa na juu ya uso lazima kuna chembe nyingi au za kutosha. ya rangi ya bluu..
Unaweza hata kuondoa uamuzi wafuatayo wa metali.
Chuma - Hii ni kipengele cha kemikali, katika muundo wa tabaka za uso ambazo kuna lazima chembe za bluu.
Lakini yasiyo ya chuma - Hii ni kipengele, katika muundo wa tabaka ya uso ambayo hakuna au karibu hakuna photons ya bluu, na lazima kuna nyekundu.
Vyuma na kivutio chao kikubwa huchukua elektroni. Na kwa hiyo wao ni mawakala wa kupunguza.
Tunatoa ufafanuzi wa dhana za "electronegacity", "kiwango cha oxidation", "redox athari", ambayo inaweza kupatikana katika vitabu vya vitabu katika kemia.
« Shahada ya oxidation. - Malipo ya masharti ya atomi katika kiwanja yaliyohesabiwa kwa misingi ya dhana kwamba inajumuisha tu ya ions. Katika kuamua dhana hii, ni kawaida kuaminiwa kwamba watengenezaji (valence) elektroni kwenda kwa atomi zaidi electronegative, na hivyo misombo inajumuisha kama ilivyokuwa kutoka ions chanya na vibaya kushtakiwa. Kiwango cha oxidation inaweza kuwa na thamani ya sifuri, hasi na chanya, ambayo huwekwa juu ya ishara ya kipengele kutoka hapo juu.
Thamani ya sifuri ya kiwango cha oxidation inahusishwa na atomi za vipengele katika hali ya bure ... Thamani hasi ya kiwango cha oxidation ina atomi hizo ambazo wingu wa elektroni (elektroni) hubadilishwa. Fluorine katika uhusiano wake wote ni sawa na -1. Kiwango cha oxidation kina atomi ambazo hutoa elektroni za valence kwa atomi nyingine. Kwa mfano, metali ya ardhi ya alkali na alkali, ni kwa mtiririko +1 na +2. Katika ions ya kawaida, ni sawa na malipo ya ion. Katika misombo nyingi, kiwango cha oxidation ya atomi hidrojeni ni + 1, lakini katika hydridi ya metali (misombo na hidrojeni) na wengine - ni sawa na -1. Kwa oksijeni, kiwango cha oksidi -2 ni tabia, lakini, kwa mfano, katika kiwanja na fluorine itakuwa +2, na katika uhusiano wa peroxidation -1. ...
Jumla ya algebra ya oxidation ya atomi katika kiwanja ni sifuri, na katika ion tata - malipo ya ion. ...
Kiwango cha juu cha oxidation ni thamani kubwa zaidi. Kwa vipengele vingi, ni sawa na idadi ya kikundi katika mfumo wa mara kwa mara na ni tabia muhimu ya kipengele katika uhusiano wake. Thamani ndogo ya kiwango cha oxidation ya kipengele, ambayo hutokea katika misombo yake, ni desturi inayoitwa kiwango cha chini cha oxidation; Wengine - kati "(kamusi ya encyclopedic ya chemist mdogo, makala" shahada ya oxidation ").
Hapa ni habari ya msingi inayohusiana na dhana hii. Ni karibu na neno lingine - "umeme".
« Umeme. - Hii ni uwezo wa atomi katika molekuli ya kuvutia elektroni inayohusika katika malezi ya dhamana ya kemikali "(kamusi ya encyclopedic ya kemia ya vijana, makala" Umeme ").
"Redox athari zinaongozana na mabadiliko katika kiwango cha oxidation ya atomi ambazo ni sehemu ya vitu vya kujibu, kama matokeo ya kuhamia elektroni kutoka atomi ya moja ya reagents (kupunguza wakala) kwa atomi nyingine. Kwa oxidative na kupunguza athari, oxidation (elektroni kurudi) na kurejesha (elektroni kuongeza) kutokea (kemikali encyclopedic kamusi) (kemikali encyclopedic kamusi Ed. I.L. Knunyantz, makala "Redox Reaction").
Kwa maoni yetu, kuna makosa machache katika dhana hizi tatu.
Kwanza , Tunaamini kwamba malezi ya uunganisho wa kemikali kati ya vipengele viwili sio mchakato wote wa jamii ya electroni zao. Kemikali Bond ni uhusiano wa mvuto. Elektroni, inadaiwa kuruka karibu na kernel, ni photons huru kukusanya juu ya uso wa nucleons katika mwili wa kipengele na kati yao. Ili kati ya vipengele viwili uunganisho uliondoka, photoni zao za bure hazihitaji kukimbia kati ya vipengele. Hii haina kutokea. Kwa kweli, kipengele kikubwa kinachukua (huvutia) picha za bure na nyepesi, na huwaacha (kwa usahihi, juu yako mwenyewe). Na eneo la kipengele nyepesi ambacho photons hizi ziliondolewa, kwa njia moja au nyingine. Kwa sababu ya kivutio katika eneo hili kinaonyeshwa kwa kiasi kikubwa. Na kipengele rahisi kinavutia sana. Hivyo dhamana ya kemikali inatokea.
Pili , Kemia ya kisasa inaona uwezo wa vipengele kuvutia electrons kupotoshwa - inverted. Inaaminika kuwa kubwa ya electronegativity ya kipengele, zaidi ana uwezo wa kuvutia elektroni yenyewe. Na fluorine na oksijeni inadaiwa inafanya vizuri - huvutia elektroni nyingine kwao wenyewe. Pamoja na vipengele vingine 6 na vikundi 7.
Kwa kweli, maoni haya sio zaidi ya udanganyifu. Inategemea mtazamo usio sahihi, kama nambari ya kikundi zaidi, vitu vikali. Na pia, kubwa zaidi malipo ya kiini. Hii ni bullshit. Wanasayansi hawana hata kujisumbua wenyewe kuelezea kwamba kutoka kwa mtazamo wao ni "malipo." Kwa tu, kama ilivyo kwa namba, walirudia mambo yote kwa utaratibu, na walisainiwa kwa mujibu wa idadi ya maadili ya malipo. Kuongezeka kwa Kubwa!
Hii ni wazi na mtoto kwamba gesi ni nyepesi kuliko chuma mnene. Je, ilitokeaje kwamba katika kemia inachukuliwa kuwa gesi ni bora kuvutia elektroni?
Metali nyembamba, bila shaka, wao ni bora kuvutia elektroni.
Wanasayansi-madaktari, bila shaka, wanaweza kuondoka dhana ya "electronegance" katika kozi, kwa kuwa ni ya kawaida. Hata hivyo, watalazimika kubadili maana yake kwa moja kwa moja.
Umeme. - Hii ni uwezo wa kipengele cha kemikali katika molekuli ili kuvutia elektroni. Na, bila shaka, katika metali, uwezo huu ni bora ulioonyeshwa kuliko yasiyo ya metali.
Kwa ajili ya miti ya umeme katika molekuli, basi, kwa kweli, pole hasi - Hizi ni mambo yasiyo ya chuma ambayo hutoa elektroni na nyanja ndogo za kivutio. Lakini chanya - Ni vipengele daima na mali zaidi ya chuma, na mashamba makubwa ya kivutio.
Tabasamu pamoja.
Umeme. - Hii ni mwingine, jaribio jingine la kuelezea ubora wa kipengele cha kemikali, pamoja na tayari kupima na malipo. Kama mara nyingi hutokea, wanasayansi kutoka eneo tofauti la sayansi, katika kesi hii, kemia, kama sio kuamini na wenzake kwa fizikia, lakini badala yake, kwa sababu tu mtu yeyote, kufanya uvumbuzi, ni kwa njia yake mwenyewe, na sio tu kuchunguza uzoefu wa wengine.
Kwa hiyo ilitokea wakati huu.
Misa na malipo hayakusaidia madawa ya kulevya kuelewa kile kinachotokea kwa atomi wakati walipokuwa wakiingiliana na kila mmoja - na electronegate ilianzishwa - uwezo wa kipengele cha kuvutia elektroni zinazohusika katika malezi ya dhamana ya kemikali. Inapaswa kutambuliwa kuwa wazo la dhana hii limewekwa kweli sana. Kwa marekebisho pekee ambayo yanaonyesha ukweli katika fomu iliyoingizwa. Kama tulivyosema, ni bora kuvutia elektroni za chuma, badala ya yasiyo ya metali - kwa sababu ya sifa za rangi ya nyukseons ya uso. Metali ni mawakala bora wa kupunguza. Nonmetals - mawakala wa oksidi. Metali huchukuliwa, zisizo za metali zinatoa. Metali - Yin, Nemmetalla - Yang.
Esoteric inakuja kusaidia sayansi katika masuala ya kuelewa siri za asili.
Kuhusu Kuhusu shahada ya oxidation. Hii ni jaribio jema la kuelewa jinsi usambazaji wa elektroni za bure unatokea ndani ya kiwanja cha kemikali - molekuli.
Ikiwa kiwanja cha kemikali ni sawa - yaani, ni rahisi, muundo wake una mambo ya aina hiyo - basi kila kitu ni kweli, kwa kweli kiwango cha oxidation ya kipengele chochote katika kiwanja ni sifuri. Kwa kuwa hakuna vioksidishaji katika uhusiano huu na hakuna rebooters. Na mambo yote ni sawa na ubora. Hakuna mtu anayechukua elektroni, hakuna mtu anayepa. Ikiwa ni dutu kubwa, au kioevu, au gesi - bila kujali.
Kiwango cha oxidation, pamoja na electronegativity, inaonyesha ubora wa kipengele cha kemikali - tu ndani ya mfumo wa kipengele cha kemikali. Kiwango cha oxidation imeundwa kulinganisha ubora wa vipengele vya kemikali katika kiwanja. Kwa maoni yetu, wazo ni nzuri, lakini utekelezaji wake haukubali kabisa.
Sisi kwa kiasi kikubwa dhidi ya nadharia nzima na dhana ya muundo wa vipengele vya kemikali na uhusiano kati yao. Naam, kama tu kwa sababu idadi ya vikundi, kulingana na mawazo yetu, inapaswa kuwa zaidi ya 8. Na kwa hiyo, mfumo wote huanguka. Ndiyo, na sio tu. Kwa ujumla, recalculate idadi ya elektroni katika atomi ya "vidole" ni kwa namna fulani si mbaya.
Kwa mujibu wa dhana ya sasa, inageuka kuwa oxidizers yenye nguvu hupewa mashtaka madogo ya masharti - fluorine ina malipo -1 katika misombo yote, oksijeni karibu kila mahali -2. Na katika metali sana - alkali na ardhi ya alkali - mashtaka haya, kwa mtiririko huo, +1 na +2. Baada ya yote, sio mantiki kabisa. Ingawa, tunarudia, tunaelewa mpango wa jumla, kwa mujibu wa ambayo ulifanyika - yote kwa ajili ya makundi 8 katika meza na elektroni 8 katika ngazi ya nishati ya nje.
Hata hivyo, kwa kiwango cha chini, ukubwa wa mashtaka haya huko Halogen na oksijeni ilipaswa kuwa kubwa zaidi na ishara ndogo. Na metali ya ardhi ya alkali na alkali pia ni kubwa, tu kwa ishara ya pamoja.
Kwa yeyote kemikali kiwanja Kuna mambo ambayo hutoa elektroni - mawakala wa oksidi, yasiyo ya metali, mashtaka hasi, na vipengele vinavyochukua elektroni - mawakala wa kupunguza, metali, malipo mazuri. Hii ndiyo njia ya kulinganisha vipengele, kuwaelezea kwa kila mmoja na kujaribu, kuamua kiwango chao cha oxidation.
Hata hivyo, ili kujua kwa njia hii kiwango cha oxidation, kwa maoni yetu, haifai kabisa ukweli. Ingekuwa sahihi zaidi kulinganisha electronegability ya vipengele katika molekuli. Baada ya yote, electronegativity ni sawa na kiwango cha oxidation (inaonyesha ubora, kipengele tofauti tu).
Unaweza kuchukua kiwango cha umeme na kuiweka kwenye formula kwa kila kipengele. Na kisha itaonekana mara moja, mambo ambayo hutolewa elektroni, na ambayo yanachukuliwa. Kipengele hicho ambacho electronegativity katika kiwanja ni pole ya juu - hasi, inatoa elektroni. Na yeye ambaye electronegability ni ndogo sana - chanya, inachukua elektroni.
Ikiwa vitu, kukubali, 3 au 4 katika molekuli, hakuna mabadiliko. Wote pia kuweka ukubwa wa electronegability na kulinganisha.
Ingawa haipaswi kusahau kuteka mfano wa muundo wa molekuli. Hakika, katika kiwanja chochote, ikiwa si rahisi, yaani, haijumuishi na aina moja ya vipengele, huhusishwa na kila mmoja, kwanza, metali na zisizo za metali. Metali Chagua elektroni katika zisizo za metali, na uwafunge. Na katika kipengele kimoja cha yasiyo ya chuma, elektroni 2 inaweza kuchaguliwa kwa wakati mmoja au idadi kubwa ya vipengele na mali zaidi ya chuma. Hivyo ngumu, molekuli tata hutokea. Lakini hii haina maana kwamba katika molekuli hiyo, vipengele vya chuma vitakuja katika uhusiano thabiti na kwa kila mmoja. Labda watakuwa kwenye pande tofauti kutoka kwa kila mmoja. Ikiwa karibu - watavutia. Lakini uhusiano imara huundwa tu ikiwa kipengele kimoja ni cha chuma zaidi kuliko nyingine. Hakikisha kufanya kipengele kimoja chagua elektroni - kuondolewa. Vinginevyo, kipengele hakitatokea - msamaha kutoka kwa picha za bure juu ya uso. Sehemu ya kivutio haitaonekana vizuri, na hakutakuwa na uhusiano wa kudumu. IT. mada tata - Elimu mahusiano ya kemikaliNa hatuwezi kusema juu yake kwa undani katika makala hii.
Tunaamini, sisi tuliacha mada ya kujitolea kwa uchambuzi wa dhana za "electronegacity", "shahada ya oxidation", "oxidation" na "marejesho", na kutolewa kwa tahadhari yako mengi ya habari.
Kutoka kwa ndoto zilizoweza kusimamia Mwandishi wa ulimwengu Elena.Marejesho "Wakati ishara ya umoja ya Indi-Appeam imezaliwa, kiini na maisha imegawanywa katika mbili. Kutoka hatua hii, ikiwa ulimwengu wa mwisho haufikii, kiini na maisha hayataona tena. " William, "Siri ya Maua ya Golden" baada ya Taasisi
Kutoka kitabu kitabu cha siri. Ni dhahiri dhahiri duniani na nje ya nchi. Mwandishi Vyatkin Arkady Dmitrievich.Masochism kama kiwango cha juu cha vampirism ya hiari kwa maana hii Masochism ni sawa na mawasiliano ya simu. Mazochists ni watu wanaopata hisia nzuri kutokana na mateso yao ya kimwili na ya akili. Kwa maneno mengine, wanaipenda wakati wanapiga, wakipiga,
Kutoka kwenye kitabu cha Vampires nchini Urusi. Wote unahitaji kujua kuhusu wao! Mwandishi Bauer Alexander.Jinsi ya kuamua kiwango cha kupoteza damu wakati vinywaji vya vampire, kisha vinywa mara moja kutoka nusu lita hadi lita moja na nusu ya damu. Mwili wa mwanadamu una lita tano tu au sita za damu, ili kupoteza damu hiyo sio hatari kwa maisha. Hata hivyo, vampire inaweza
Kutoka kwa kitabu kinachoonyesha wakati ujao katika ndoto. Mwandishi wa ulimwengu Elena.Marejesho Baada ya usambazaji wa taasisi, kufanya kazi kama mhandisi katika kampuni iliyofungwa, nilitambua kuwa sikuwa katika nafasi yangu, kwa hiyo niliamua kubadili taaluma na kuingia shule ya jazz ya improvisation, na baadaye katika shule ya muziki kwa ofisi ya classic .
Kutoka kitabu cha dhahabu sheria Fengshui. Hatua 10 rahisi za kufanikiwa, ustawi na uhai Mwandishi Rudin Valentin Leonidovich.Kiwango cha athari mbaya ya vitu vya nje ni madhara makubwa ya nje ya nje, kuwa mara moja kabla ya kuingia nyumbani. Lakini zaidi wao iko kwenye pembe kwa mlango, dhaifu huwa na ushawishi wao. Kitu ni moja kwa moja
na mwandishi wa Eduard tiba.Shahada ya kwanza: kupikia. Mahubiri ya Nagorny na ufalme wa Mungu wa Kristo huanza na Galilaya Idyll na kutangazwa kwa "ufalme wa Mungu." Utabiri huu unaonyesha sisi kwa maelekezo yake maarufu. Wakati huo huo, ni maandalizi ya kuinua zaidi
Kutoka kitabu cha mageuzi ya Mungu. Kutoka Sphinx kwa Kristo. na mwandishi wa Eduard tiba.Shahada ya pili ya uanzishwaji (utakaso). Uponyaji wa ajabu. Tiba ya Kikristo katika siri zote za kale za maandalizi ya maadili na kiakili zinapaswa kutakasa nafsi, ambayo inapaswa kufufua viungo vipya ndani yake na kuipa hatimaye uwezo
Kutoka kwenye kitabu cha kitendawili cha Sphinx Mwandishi wa Barbaren Georges.Marejesho ya sanamu umri halisi wa sphinx kubwa hurudi mwanzo wa zama za Adamu. Angalau yeye ni piramidi ya kisasa, mfano ambao yeye, kama tutakavyoona, alikamilisha. Picha ya Sphynx kubwa imekuwa chini ya karne ya muda
Kutoka kwa uponyaji wa kitabu cha nafsi. Mbinu 100 za kutafakari, mazoezi ya uponyaji na utulivu. Mwandishi Rajnish Bhagwan Sri.Marejesho ya rhythm ... Sakinisha wakati huo huo kwenda kulala - ikiwa kila jioni ni kumi na moja, inamaanisha kuwa kumi na moja. Hii ndiyo ya kwanza: kupata muda fulani, na hivi karibuni mwili utaweza kuingia rhythm hii. Usibadili wakati huu, vinginevyo utachagua mwili. Mwili.
na mwandishi KuzMishin E. L.Shahada ya mapokezi ya mwanafunzi kwa shahada ya mwanafunzi. Mapambo ya makao ya wageni na domains na dari ya nyumba ya wageni inapaswa kuoka sura ya bluu na nyeupe bila ya kuigiza. Juu ya mkuu wa mtaalam Mwalimu iko kuzungukwa na uangazaji wa pembetatu na jina katika kituo chake
Kutoka Kitabu cha Calisostro na Freemasonry ya Misri. na mwandishi KuzMishin E. L.Mapokezi katika shahada ya mwanafunzi. Mapambo ya makaazi na domains na dari ya nyumba ya wageni inapaswa kuwekwa na suala la bluu na nyeupe bila kuifunga. Juu ya mkuu wa mtaalam Mwalimu iko kuzungukwa na uangazaji wa pembetatu na jina "Yehova", amefungwa katikati yake
Kutoka kwa kitabu cha autobiography yoga. Mwandishi Yogananda Paramyansa.Sura ya 23 Ninapata shahada ya Chuo Kikuu - unapuuza ufafanuzi wa falsafa kutoka kwa kitabu cha maandishi bila shaka kuhesabu kwamba baadhi ya "intuition" isiyo ya kuzunguka itakushika kupitia mitihani yote. Lakini ikiwa unashauriana kwa njia ya kisayansi zaidi, basi nitahitaji
Kutoka Kitabu cha Kabbalah. Dunia ya juu. Mwanzo wa njia Mwandishi Mwanga Michael.7.5. Kiwango cha ufahamu wa uovu kama ilivyofafanuliwa katika makala "Kujishughulisha", radhi na furaha hutegemea kiwango cha kufanana kwa Muumba kulingana na mali, na mateso na uvumilivu - kiwango cha tofauti kutoka kwa Muumba. Kwa mujibu wa hili, egoism ni kuchukiza kwetu na rangi isiyo na rangi,
Chaguo 1
1. Tambua kiwango cha oxidation ya atomi ya vipengele vya kemikali katika uhusiano wafuatayo: HNO₃, NO₂, H₃N, SO₂, N₂O.
2. Kuchukua faida ya meza ya mara kwa mara, nafasi ya vipengele vifuatavyo ili kupunguza electronegativity: o, n, kuwa, B, li, C. Kuamua ambapo fluorine na sodiamu inapaswa kuwa katika mstari huu. Eleza jibu. 
3. Kiwango cha oxidation ya atomi ya sulfuri kinabadilikaje wakati wa hivyo? Jibu kuelezea jibu.
Chaguo 2.
1. Kuamua kiwango cha oxidation ya atomi ya vipengele vya kemikali katika uhusiano wafuatayo: co₂, h₃po₄, sih₄, p₂o₅, mg₂si.
2. Katika mwelekeo wa atomi ya kipengele cha kemikali kinabadilishwa kwa ujumla wanandoa wa elektroniki., Molekuli ya uhusiano wafuatayo: BF₃, PCL₃, CS₂, CCL₄, HBR? Kutoa jibu la busara.
3. Ikiwa kiwango cha mabadiliko ya oksidi ya kaboni wakati wa malezi asidi ya Coaltic. H₂co₃ kaboni dioksidi na maji? Jibu kuelezea jibu.
Chaguo 3.
1. Kuamua kiwango cha oxidation ya atomi ya vipengele vya kemikali katika uhusiano wafuatayo: Cl₂, Naclo, Cacl₂, HF, Soo, Cl₂o₇.
2. Kutumia mfumo wa mara kwa mara Vipengele vya kemikali, nafasi ya vipengele vifuatavyo kwa utaratibu wa kuongeza umeme wao: P, al, cl, na, s, mg. Pata potasiamu na fluorine katika safu hii. Jibu kuelezea jibu. 
3. Kiwango cha oksidi cha kaboni kinabadilikaje wakati wa kuchoma methane ch₄ na kuundwa kwa oksidi ya kaboni (IV) na maji? Jibu kuelezea jibu.
Chaguo 4.
1. Tambua kiwango cha oxidation ya atomi ya vipengele vya kemikali katika uhusiano wafuatayo: H₂SO₄, SO₂, NO₂, BF₃, H₂S.
2. kuelekea atomi ambazo vipengele vya kemikali Inaonyesha jozi za elektroniki za jumla, katika molekuli ya uhusiano wafuatayo: H₂o, PCL₃, H₃N, H₂S, CO₂? Kutoa jibu la busara.
3. Ikiwa digrii za oxidation ya atomi zinabadilishwa wakati maji yamebadilishwa kutoka dutu rahisi - hidrojeni na oksijeni? Jibu kuelezea jibu.


