Задачи повышенной сложности*. Физика атома и ядра.
1 ) Радиус первой орбиты в атоме водорода r 1 = 5.3-10 -11 м. Найти напряженность электрического поля ядра на этом расстоянии и кинетическую энергию электрона на этой орбите.
Решение:
Напряженность электрического поля найдем по формуле
где
После подстановки числовых значений получим Е =5.1·10 11 В/м.
Чтобы найти второй параметр, запишем второй закон Ньютона, принимая во внимание тот факт, что на электрон действует кулоновская сила притяжения
которая сообщает ему центростремительное ускорение
где
v
— скорость движения электрона. Итак, получаем уравнение 
Следовательно, кинетическая энергия электрона 
Ответ:
W
k =13.6 эВ.
2) Во сколько раз увеличится радиус орбиты электрона у атома водорода, находящегося в основном энергетическом состоянии, при поглощении атомом фотона с энергией 12. 09 эВ?
Решение:
Согласно теории Бора, полная энергия атома водорода равна сумме кинетической энергии электрона и потенциальной энергии электростатического взаимодействия между электроном и протоном ядра, причем в любом энергетическом состоянии

В основном состоянии  При поглощении фотона атом водорода переходит в состояние с большей энергией С другой стороны,
При поглощении фотона атом водорода переходит в состояние с большей энергией С другой стороны,  где
r
n
— радиус орбиты электрона.
где
r
n
— радиус орбиты электрона.
Тогда 
Радиус орбиты электрона увеличится в 9 раз.
Ответ:
в
9 раз.
3) Первоначально невозбужденный водород начнет излучать фотоны, если через него пропустить пучок электронов, прошедших разность потенциалов и 0 —10. 2 В. Какую минимальную ускоряющую разность потенциалов должен пройти пучок протонов, чтобы при пропускании их через первоначально невозбужденный водород последний начал излучать фотоны? Считать, что масса электрона много меньше массы протона, а атом водорода перед столкновением покоился.
Решение:
Пусть масса налетающей частицы
т,
ее скорость v
0 , масса атома водорода М
, скорости частиц после столкновения
v 1
и
v 2
.
По закону сохранения импульса ![]() .
При столкновении атом водорода поглощает энергию
W n,h ,
поэтому по закону сохранения энергии
.
При столкновении атом водорода поглощает энергию
W n,h ,
поэтому по закону сохранения энергии

Получаем систему уравнений:

Докажем, что энергия налетающей частицы будет минимальна, если после, столкновения частица и атом водорода движутся с одинаковыми скоростями (абсолютно неупругое столкновение). Выразим из первого уравнения системы  и подставим во второе уравнение, тогда получим:
и подставим во второе уравнение, тогда получим:

Таким образом, энергия налетающей частицы
W
0
выражена как квадратичная функция от v
1 с первым положительным коэффициентом

Такая функция имеет минимум в точке где
 Итак, скорость, соответствующая минимуму
W
0
:
Итак, скорость, соответствующая минимуму
W
0
:

При этом
Итак, доказано, что энергия налетающей частицы минимальна, если после столкновения частицы движутся с одинаковыми скоростями, т.е. v 1 =v 2 . Минимальное значение энергии налетающей частицы

В случае, когда через водород пропускают электроны, ![]() поэтому
поэтому ![]() т.е. вся энергия электронов поглощается водородом, который переходит в возбужденное состояние. Электроны приобретают энергию, пройдя ускоряющую разность потенциалов и
0 , т.е.
т.е. вся энергия электронов поглощается водородом, который переходит в возбужденное состояние. Электроны приобретают энергию, пройдя ускоряющую разность потенциалов и
0 , т.е.
В случае, когда через водород пропускают протоны, отношение т/М= 1, поэтому минимальная энергия налетающих протонов
Таким образом, минимальная ускоряющая разность потенциалов для протонов равна 20,4 В.
Ответ:
20.4 В.
4) Какие спектральные линии появятся при возбуждении атомарного водорода электронами с энергией W =12. 1 эВ?
Решение:
Вся энергия электронов поглощается водородом, который возбуждается и переходит из основного энергетического состояния с
п
=1 в некоторое состояние, характеризуемое натуральным числом k
.
По закону сохранения энергии
![]() С другой стороны:
С другой стороны:  где
W
ион
=
13.
6 эВ. Получаем уравнение
где
W
ион
=
13.
6 эВ. Получаем уравнение

Иэ состояния с k =3 возможен прямой переход в состояние с п =1 или п= 2, а также переход со второго энергетического уровня на первый. Таким образом, получится три спектральных линии. Рассчитываем соответствующие длины волн, используя формулу

Переходу из состояния с
k
=3 в состояние с
n=
1 соответтвует спектральная линия с длиной волны
Переходу из состояния с
k
=3 в состояние
с
п
=2
соответствует спектральная линия с длиной волны
Переходу из состояния с
k
=2 в состояние с n
=1 соответствует спектральная линия с длиной волны
5)
Напряженность электрического поля в электромагнитной волне с частотой ![]() модулированной по амплитуде с частотой
модулированной по амплитуде с частотой ![]() меняется со временем по закону:
где А
— постоянная. Определить энергию электронов, выбиваемых этой волной из атомов газообразного водорода с энергией ионизации
W
ион =13.6 эВ.
меняется со временем по закону:
где А
— постоянная. Определить энергию электронов, выбиваемых этой волной из атомов газообразного водорода с энергией ионизации
W
ион =13.6 эВ.
Решение:
Преобразуем выражение для напряженности электрического поля:
Таким образом, модулированная по амплитуде волна представляет собой сумму трех монохроматических волн с частотами В соответствии с постулатами Бора атом водорода может излучать и поглощать электромагнитную энергию только определенными порциями (квантами). Вычислим кванты энергии, соответствующие найденным монохроматическим волнам.
Для волны с частотой 
Для волны с частотой ![]()

Для волны с частотой ![]()

Энергия ионизации атома водорода и, как видно, она больше, чем
Поэтому кванты с частотами ![]() не могут ионизировать атом водорода. Ионизацию вызывает только квант с частотой
и по закону сохранения энергии энергия выбитых этим квантом электронов
не могут ионизировать атом водорода. Ионизацию вызывает только квант с частотой
и по закону сохранения энергии энергия выбитых этим квантом электронов
Ответ: W e = 0.88 эВ.
6) В периодической таблице рядом расположены три элемента X, У, S . Радиоактивный изотоп элемента X превращается в элемент У , а тот, в свою очередь, — в элемент S . Последний превращается в изотоп исходногоα -распад.
7) Ядро нептуния после α и β -распадов превращается в ядро висмута. Какое число α и β -распадов происходит при этом?
Решение:
В результате распадов массовое число изменяется на 237 - 209 = 28 атомных единиц. Как известно, при β -распаде масса ядра не изменяется, следовательно, изменение массового числа происходит только за счет α -распадов. При одном α -распаде массовое число изменяется на 4 атомные едини-цы, значит, должно произойти 28/4 = 7 α -распадов. При этом заряд ядра должен уменьшиться на 7·2 = 14 элементарных зарядов. В нашем случае уменьшение заряда ядра равно 93 - 83 = 10. Следовательно, в результате β -распадов заряд увеличился на 14 - 10 = 4 элементарных заряда. Так как при одном β -распаде заряд ядра увеличивается на 1 элементарный заряд, то должно произойти 4/1 = 4 β -распада.
Излучение и поглощение энергии атомами. Структура энергетических уровней атомов. Оптические спектры атома водорода и спектры сложных атомов.
Структура энергетических уровней сложных молекул. Молекулярные спектры.
Эмиссионный и абсорбционный спектральный анализ, его медицинское применение. Спектроскопы, спектрографы, монохроматоры, спектрофотометры и их применение в медицине.
Люминесценция, ее виды. Характеристики люминесценции (спектр, длительность, квантовый выход). Законы Вавилова и Стокса. Люминесцентный анализ. Люминесцентные метки и зонды. Медицинское применение люминесцентных методов исследования.
Излучение и поглощение энергии атомами и молекулами.
В 1913 году Бором предложена теория излучения света, которая основывается на двух постулатах.
Внутренняя энергия атома дискретна, то есть может принимать только определённые дозволенные значения или уровни, кратные характерным для данного атома количествам, или квантам энергии. Состояния атома, соответствующие этим уровням энергии, являются стационарными: в таком состоянии атом не излучает электромагнитных волн, несмотря на происходящее в нём движение электронов.
Испускание (или поглощение) электромагнитного излучения происходит при переходе атома из одного стационарного состояния в другое. При этом испускается (или поглощается) фотон монохроматического излучения с энергией, равной разности энергетических уровней Е m иE n , соответствующих этим состояниям:
h = E m - E n ,
где E m иE n - энергия системы в первом и втором состояниях.
На основе этих постулатов Бор разработал теорию излучения и поглощения энергии света атомом водорода. Он предположил, что из всех возможных орбит электрона осуществляются только те, для которых момент импульса (момент количества движений) равен целому кратному постоянной Планка, делённой на 2 :
(n = 1, 2, 3, . . .) . (1.)
Число n , называется главным квантовым числом, соответствует порядковому номеру орбиты.
В случае атома водорода кулоновская сила взаимного притяжения протона и электрона является центростремительной силой, удерживающей электрон на орбите, то есть:
 ,
(2)
,
(2)
где m и е - масса и заряд электрона,r - радиус орбиты.
Исключая v из (1) и (2), получим, что радиус электронных орбит в атоме может принимать лишь ряд дискретных значений:
из (1)
 подставляем в (2)
подставляем в (2) откуда
откуда ,
,
(n = 1, 2, 3, ...).
Таким образом, радиусы орбит стационарных атома водорода прямо пропорциональны квадрату квантового числа n 2 .
Для первой, основной, орбиты n
= 1
и радиус ,
то есть величина порядка газокинетических
размеров атома.
,
то есть величина порядка газокинетических
размеров атома.
Из рассмотренных соотношений находится
и скорость движения электрона по
стационарной орбите
 .
Для основной орбиты атома водорода (n
= 1):
.
Для основной орбиты атома водорода (n
= 1): 2,310 8 см/сек.
Таков порядок скорости движения
электронов по орбите.
2,310 8 см/сек.
Таков порядок скорости движения
электронов по орбите.
Энергетический уровень атома обусловлен полной энергией электрона, которая слагается из кинетической энергии электрона (ядро неподвижно) и энергии взаимодействия электрона с ядром (потенциальной энергии). Потенциальная энергия электрона (по знаку она отрицательна как потенциальная энергия сил притяжения):
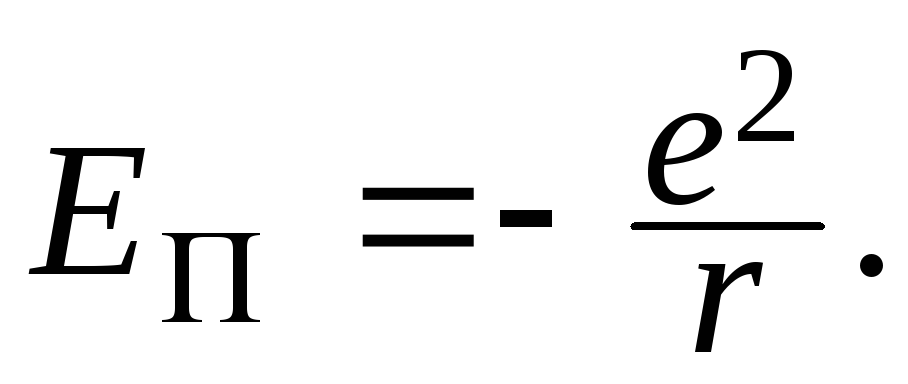
Полная внутренняя энергия:
Е
Э
=
учитывая, что
 ,
,
находим: Е
Э
=
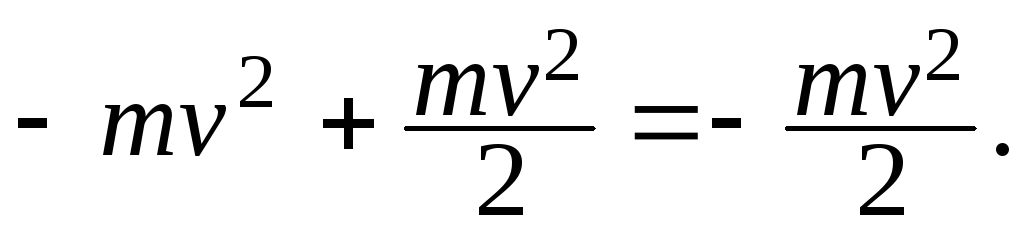
Таким образом, энергия электрона, связанного в атоме с ядром, отрицательна. Энергия же свободного электрона равна нулю.
Подставляя в это выражение значения скорости электрона, находим:
Е
Э
=
 (3)
(3)
Для атома водорода получаются следующие значения:
основной (нулевой) уровень, n = 1, Е 1 = - 13,55 эВ;
n = 2, Е 2 = - 3,38 эВ;
n = 3, Е 3 = - 1,5 эВ.
Схема энергетических уровней атома водорода представлена на рисунке.

E электрона =0
Рис. 1. Структура энергетических уровней атома водорода.
Поскольку энергетические уровни обратно пропорциональны квадрату квантового числа n 2 , разность между каждыми двумя соседними уровнями по мере возрастания числа и по абсолютной величине уменьшается. Таким образом, по мере удаления от ядра разность между двумя соседними энергетическими уровнями атома убывает:
E 2 - E 1 > E 3 - E 2 > E 4 - E 3 ,. . .
Стационарный уровень с наименьшей энергией называется основным, он соответствует состоянию атома, не подвергающегося никаким внешним воздействиям. Остальные стационарные уровни называются возбуждёнными.
Возбуждение атома, то есть переход электрона на орбиту большего радиуса (Рис. 1., путь 1), требует сообщения атому дополнительной энергии и, следовательно, происходит в результате каких-либо внешних воздействий, например, при соударении частиц в процессе интенсивного теплового движения или при электрическом разряде в газах, при поглощении фотона электромагнитного излучения, в результате рекомбинации ионов в газе или электронов и дырок в полупроводнике, при действии на атом частиц радиоактивного излучения и т.д.
Возбужденное состояние неустойчиво, примерно через 10 -8 сек электрон возвращается на основную орбиту, при этом излучается фотон, уносящий дополнительную энергию, полученную при возбуждении, и атом переходит в основное состояние (Рис.1., путь 2).
Электрон может возвращаться на основную орбиту не только единым переходом, но и ступеньками через промежуточные уровни. В этом случае при переходе будет излучаться несколько фотонов (Рис. 1., путь 3) с частотами, соответствующими разности энергий этих уровней.
Зависимость величины излучаемой атомами или молекулами энергии от длины волны или частоты световой волны называется спектром испускания , а поглощаемой -спектром поглощения . Интенсивность спектральных линий определяется числом одинаковых переходов, происходящих в единицу времени, и поэтому зависит от количества излучающих (поглощающих) атомов и вероятности соответствующего перехода.
Атомными спектрами называют как спектры испускания, так и спектры поглощения, которые возникают при квантовых переходах между уровнями свободных или слабо взаимодействующих атомов. Атомные спектры линейчаты.
Постулаты Бора. Испускание и поглощение атомов
 Предположим, что атомы некоего газа могут находиться только в состояниях с энергетическими уровнями, показанными на рисунке. В начальный момент времени атомы находятся в состоянии с энергией Е
2 . Согласно постулатам Бора, испускаемый таким газом свет может содержать фотоны с энергией
Предположим, что атомы некоего газа могут находиться только в состояниях с энергетическими уровнями, показанными на рисунке. В начальный момент времени атомы находятся в состоянии с энергией Е
2 . Согласно постулатам Бора, испускаемый таким газом свет может содержать фотоны с энергией


