Механизм излучения
Запрещённая линия нейтрального водорода обусловлена взаимодействием магнитных моментов электрона и протона в атоме водорода. Энергия атома водорода при параллельном расположении магнитных моментов электрона и протона несколько больше, чем при антипараллельном, поэтому при спонтанном изменении ориентации магнитного момента электрона на противоположную атом излучает квант электромагнитного излучения с длиной волны 21,1 см (частота 1420,40575 МГц). Параллельно с излучением радиолинии происходит и обратный процесс - возбуждения атомов водорода электромагнитными квантами с бо́льшими энергиями, например, оптическими, либо в актах соударения атомов. Поэтому в межзвёздном атомарном водороде устанавливается динамическое равновесие между актами излучения радиоквантов и возбуждением атомов оптическими квантами и соударениями.
Такой самопроизвольный переход в каждом отдельном атоме происходит крайне редко - в среднем один раз за 11 миллионов лет (1 км³ водорода при плотности 1 атом/см³ излучает всего 3 кванта в секунду), и энергия каждого кванта крайне мала из-за низкой частоты (h ν ≈ 0,941171·10 −24 Дж, или 5,87433 мкэВ ), поэтому интенсивность радиоизлучения межзвёздной среды на единицу объёма ничтожно мала. Например, мощность излучения всего водорода Солнечной системы (в пределах орбиты Плутона) составляет порядка 100 ватт . Однако в галактических масштабах мощность радиоизлучения нейтрального водорода становится заметной (например, мощность излучения всего нейтрального водорода нашей Галактики в десятки раз больше светимости Солнца), что позволяет обнаруживать его на галактических расстояниях. Это излучение крайне важно для изучения методами радиоастрономии распределения нейтрального водорода в Галактике, движения его облаков.
Значение линии нейтрального водорода в радиоастрономии
Линия нейтрального водорода является важнейшей в радиоастрономии. Более половины массы межзвёздного вещества составляет нейтральный водород. Его можно исследовать только по излучению в линии 21 см. Поэтому наблюдения излучения с длиной волны 21 см даёт очень ценные, часто уникальные, сведения о распределении нейтрального водорода в космическом пространстве. Принципиальная возможность излучения межзвёздным водородом радиолинии 21 см показана в 1945 году X. К. ван де Хюлстом . В 1948 году советский астрофизик И. С. Шкловский рассчитал ожидаемую интенсивность излучения межзвёздного водорода и показал, что она достаточна для того, чтобы его можно было обнаружить методами радиоастрономии. В 1951 году радиолиния нейтрального водорода была экспериментально обнаружена почти одновременно Х. Юэном и Э. Парселлом в США и Х. Мюллером и Я. Оортом в Нидерландах . Исследование излучения нейтрального водорода позволили получить информацию о структуре галактики: выяснилось, что большая часть нейтрального водорода сосредоточена в очень тонком (по сравнению с диаметром) слое толщиной около 220 парсек в плоскости Галактики . В распределении водорода отчётливо выделяются спиральные рукава, которые прослеживаются до больших расстояний. Измерение доплеровского смещения позволяет измерить скорость облаков нейтрального водорода относительно Земли (в том числе и красное смещение дальних галактик).
Поиск внеземных цивилизаций
Длина волны 21 см, как самая распространённая во Вселенной, выбрана в качестве рабочей для поисков внеземных цивилизаций по программе
В середине XVIII в. Г.Кирхгоф обнаружил: свечение газов дает четко выраженные дискретные линии. Швейцарский преподаватель И.Бальмер эмпирически вывел формулу для спектра водорода (1885): , гдеn – любое целое число >2, т.е. n = 3, 4, 5 и т.д.
Так как
 ,
то
,
то ,
гдеR
– постоянная Ридберга.
,
гдеR
– постоянная Ридберга.
Затем Ф. Пашен:
 n
= 4, 5, 6, ... (инфракрасное излучение),
n
= 4, 5, 6, ... (инфракрасное излучение),
Т .
Лайман:
.
Лайман: n
= 2, 3, 4, ... (ультрафиолетовое излучение).
n
= 2, 3, 4, ... (ультрафиолетовое излучение).
Значения длин волн спектральных линий, вычисленных по этим формулам, совпадали с исключительной точностью со значениями длин воли этих линий, измеренных экспериментально. В конце XIX в, ученые обнаружили фундаментальную закономерность в микромире, которую в то время объяснить не смогли. Только через 30 лет Н.Бор дал физическую интерпретацию этой формулы. Он предположил, что два члена в формуле Бальмера представляют собой полные энергии разрешенных орбит электрона в атоме водорода. Преобразовав формулу Бальмера (умножив обе части на hc ), получим
![]() ,
,
 .
.
Свои постулаты Н.
Бор применил для построения теории
атома водорода: электроны могут двигаться
в атоме только по определенным орбитам,
которые определяются условиями:
 ,
,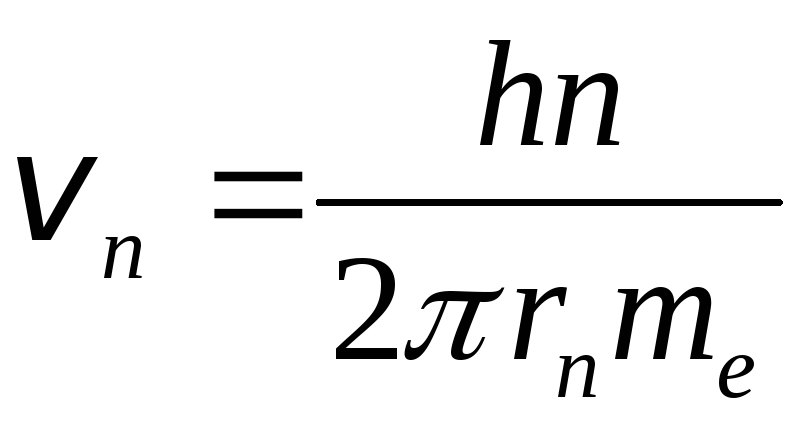 ,
гдеr
n
– радиус n
-й
орбиты; v
n
– скорость электрона на этой орбите;
m
e
– масса электрона; m
e
v
n
r
n
– момент импульса электрона; n
– целое число (n
≠0).
,
гдеr
n
– радиус n
-й
орбиты; v
n
– скорость электрона на этой орбите;
m
e
– масса электрона; m
e
v
n
r
n
– момент импульса электрона; n
– целое число (n
≠0).
Энергия кванта раина разности энергий стационарных состояний электрона: hν = E 2 −E 1 .
На электрон со
стороны ядра действует кулоновская
сила (F
K),
сообщая ему центростремительное
ускорение. Поэтому F
K
= ma
,
 ,
,
 .
.
Подставляя уравнение для скорости электрона на орбите в предыдущее, получим
 ,
где n
= 1, 2, 3, ...
,
где n
= 1, 2, 3, ...
Если n
=1,
а r
1 ≈0,5∙10 −10
м, то r
2
= r
1 n
2
= 4
r
1 ,
r
3
= 9
r
1
на основании r
1:r
2:r
3 ,
как

Полная энергия
атома равна: Е
= Е
к
+ Е п,
 ,
, ,
,

П ереход
электрона с более высокой орбитыk
на орбиту n
сопровождается излучением фотона с
частотой:
ереход
электрона с более высокой орбитыk
на орбиту n
сопровождается излучением фотона с
частотой:
 ,
,
 .
.
Таким образом, мы
пришли к формуле Бальмера, где
 .
.
Трудности теории Бора
Правило квантования Бора применимо не всегда. Представление об определенных орбитах, по которым движется электрон в атоме Бора, оказалось условным. Теория Бора неприменима для многоэлектронных атомов и не объясняет ряд спектральных закономерностей.
В 1917 г. А. Эйнштейн предсказал возможность
вынужденного излучения света атомами:
переход атома с высшего энергетического
состояния в низшее под влиянием внешнего
воздействия
1917 г. А. Эйнштейн предсказал возможность
вынужденного излучения света атомами:
переход атома с высшего энергетического
состояния в низшее под влиянием внешнего
воздействия
Излучение атома водорода
Фотон, имеющий энергию hν , возбуждает атом и переводит электрон в состояние с более высокой энергией. Электрон произвольно возвращается в первоначальное состояние, испуская фотон энергией hν .
Вынужденное излучение
П адающий
фотон с энергиейhν
взаимодействует с атомом, находящимся
в возбужденном состоянии, и стимулирует
его высвечивание. Возникают два фотона
с энергией hν
каждый, которые движутся в одном
направлении и одной фазе.
адающий
фотон с энергиейhν
взаимодействует с атомом, находящимся
в возбужденном состоянии, и стимулирует
его высвечивание. Возникают два фотона
с энергией hν
каждый, которые движутся в одном
направлении и одной фазе.
Населенность уровней
В условиях теплового равновесия большая
часы, атомов обладает минимумом энергии,
населенность верхних уровней меньше
населенности нижних. Под влиянием
энергетических воздействий (повышение
температуры, освещение) возбуждение
атомов возрастает и населенность верхних
уровней увеличивается, но получить
распределение частиц по уровням, при
котором населенность верхних уровней
больше, чем нижних, таким способом
невозможно, так как увеличение населенности
верхних уровней способствует увеличению
спонтанных переходов на нижний уровень.
Атомы могут находиться в возбужденном
состоянии 10 −8
с.
условиях теплового равновесия большая
часы, атомов обладает минимумом энергии,
населенность верхних уровней меньше
населенности нижних. Под влиянием
энергетических воздействий (повышение
температуры, освещение) возбуждение
атомов возрастает и населенность верхних
уровней увеличивается, но получить
распределение частиц по уровням, при
котором населенность верхних уровней
больше, чем нижних, таким способом
невозможно, так как увеличение населенности
верхних уровней способствует увеличению
спонтанных переходов на нижний уровень.
Атомы могут находиться в возбужденном
состоянии 10 −8
с.
Ч тобы
получить когерентное излучение в
результате вынужденного испускания,
необходимы два условия:
тобы
получить когерентное излучение в
результате вынужденного испускания,
необходимы два условия:
1 . Населенность верхних уровней должна быть больше, чем нижних.
2 .
Один из верхних уровней с состоянием
E
2
должен быть метастабильным, т.е. электроны
в нем должны находиться не 10 −8
с, а порядка, 10 −5
– 10 −3 ,
с. Уровень с состоянием E
2
мета-стабильный. Если вещество (например,
кристалл рубина) длительное время
освещать, то произойдет очень плотное
заселение метастабильных уровней. При
наличии уровня с состоянием E
2
возможны спонтанные переходы из состояния
E
3
не только в основное состояние E
1 ,
но и на метастабильный уровень с
состоянием E
2 .
Оба перехода сопровождаются выделением
энергии. Большое различие во временах
жизни в состояниях E
3
и Е
2
приводит к тому, что под действием
возбуждающих фотонов с энергией hν≥E
3 –Е
1
атомы переходят в состояние Е
3 ,
а затем самопроизвольно – в состояние
Е
2 .
Без излучения света (энергия поглощается
кристаллом) и происходит накопление
атомов на метастабильном уровне с
состоянием E
2 .
Для создания в лазере инверсной
населенности используют Al 2 O 3
смесь гелия (15%), неона (85%) и другие
вещества. Переход из состояния E
2
в состояние E
1
под действием внешней электромагнитной
волны сопровождается излучением, что
и используется в лазерах.
.
Один из верхних уровней с состоянием
E
2
должен быть метастабильным, т.е. электроны
в нем должны находиться не 10 −8
с, а порядка, 10 −5
– 10 −3 ,
с. Уровень с состоянием E
2
мета-стабильный. Если вещество (например,
кристалл рубина) длительное время
освещать, то произойдет очень плотное
заселение метастабильных уровней. При
наличии уровня с состоянием E
2
возможны спонтанные переходы из состояния
E
3
не только в основное состояние E
1 ,
но и на метастабильный уровень с
состоянием E
2 .
Оба перехода сопровождаются выделением
энергии. Большое различие во временах
жизни в состояниях E
3
и Е
2
приводит к тому, что под действием
возбуждающих фотонов с энергией hν≥E
3 –Е
1
атомы переходят в состояние Е
3 ,
а затем самопроизвольно – в состояние
Е
2 .
Без излучения света (энергия поглощается
кристаллом) и происходит накопление
атомов на метастабильном уровне с
состоянием E
2 .
Для создания в лазере инверсной
населенности используют Al 2 O 3
смесь гелия (15%), неона (85%) и другие
вещества. Переход из состояния E
2
в состояние E
1
под действием внешней электромагнитной
волны сопровождается излучением, что
и используется в лазерах.
В 1940 г. В.А.Фабрикант указал на возможность использования вынужденного излучения для усиления электромагнитных волн.
Отечественные ученые Н.Г.Басов и А.М.Прохоров изобрели микроволновый генератор (лазер) (1954) и получили Нобелевскую премию.
Лазеры
Путем внешнего освещения возбужденные электроны из состояний E 2 и E 3 переходят в состояние E 1 , которое является рабочим состоянием лазера.
Лазерное излучение может быть различного цвета.
Рубиновый лазер генерирует пучок фотонов (λ = 694 нм) рубиново-красного света.
Учебник для 10 класса
§27.4. Нейтральный водород
Водород в светлых туманностях ионизуется и светится, только если поблизости есть горячие звезды. Но основная масса водорода в Галактике нейтральна . Нейтральный водород в космосе не светится и невидим. Однако он излучает радиоволну длиной 0,21 м. По интенсивности излучения на этой длине волны определяют массу и плотность водорода, а по отличию фактической длины волны от 0,21 м по принципу Доплера - Физо определяют скорость водородного облака. В настоящее время выяснена общая картина распределения водорода в Галактике (рис. 97). Он расположен преимущественно в тонком слое вблизи галактической плоскости Облака водорода можно наблюдать на расстояниях, гораздо больших, чем те, на которых возможно наблюдать в телескоп отдельные звезды. Температура облаков нейтрального водорода в среднем менее 100 К, а температура ионизованных светящихся облаков (туманностей) около 10000 К. В плотных газовых облаках атомы водорода объединяются в молекулы Н 2 . Полная масса межзвездного водорода составляет несколько процентов от общей массы Галактики, а масса космической пыли еще в 100 раз меньше. Плотность нейтрального водорода в плоскости Галактики составляет в среднем около 10 -21 кг/м 3 .

Рис. 97. Распределение плотности нейтрального водорода в плоскости Галактики на различных расстояниях от ее центра.
В межзвездном пространстве помимо водорода находятся гелий, а также атомы и некоторые простейшие молекулы других химических элементов в количестве, малом сравнительно с водородом и гелием. Многие молекулы обнаружены радиометодами (по излучению и поглощению радиоволн) Среди них ОН, Н 2 0, СО, С0 2 , NH 3 и некоторые более сложные молекулы.
Методические указания
К выполнению лабораторной работы
ЕТИ.Ф. 03
Егорьевск 2003
Составитель: ст. преп. Никифоров В.Ю.
Рецензент доцент к.ф-м.н. Бурмистров А.В.
В методических указаниях рассмотрены: развитие представлений о строении атома, модели строения атома: модель Томпсона и планетарная модель Резерфорда, постулаты Бора, знакомство с квантовой моделью атома при моделировании процесса испускания электромагнитного излучения возбужденными атомами водорода, экспериментальное подтверждение закономерностей формирования линейчатого спектра излучения атомарного водорода при низких давлениях и экспериментальное определение постоянной Ридберга с использованием компьютерных моделей программы ООО «Физикон» «Открытая физика 1.1» версия «Виртуальный практикум по физике для ВУЗов». В основе данных методических указаний лежит учебное пособие «Тихомиров Ю.В. Лабораторные работы по курсу физики с компьютерными моделями (Квантовая физика). Учебное пособие для студентов высших технических учебных заведений дневной, вечерней и заочной (дистанционной) форм обучения. -М.:2003.-22 с.» Методические указания предназначены для студентов 2 вузовского курса, обучающихся по специальностям 120100, 120200, 330200,210200.
Методические указания обсуждены на заседании кафедры естественно-научных дисциплин.
Протокол № от
Заведующий кафедрой А.П. Нилов
Методические указания рассмотрены и одобрены методическим советом института
Протокол № от
Председатель совета А.Д.Семенов
Изучение спектра излучения атомарного водорода
1 Цель работы Знакомство с планетарной и квантовой моделями атома при моделировании процесса испускания электромагнитного излучения возбужденными атомами водорода.
Экспериментальное подтверждение закономерностей формирования линейчатого спектра излучения атомарного водорода при низких давлениях.
Экспериментальное определение постоянной Ридберга.
2 Оборудование: компьютерный класс, пакет прикладных программ для поддержки лабораторного практикума компании ООО «ФИЗИКОН» «Виртуальный практикум для ВУЗов».
3.1 Изучение теоретического материала, с использованием конспекта лекций и учебника.
3.2 Запуск программы: выбрать «Квантовая физика» и «Постулаты Бора». Ознакомление с краткими теоретическими сведениями программы. Запись необходимого в конспект.
3.3 Отметить маркером мыши уровень энергии электрона с номером n 0 , указанным в таблице 2 для вашей бригады.
3.4 Наблюдение и зарисовывание модели атома водорода (в левом верхнем поле), а также стрелок в правом поле и отметки в нижнем поле, соответствующих линиям в данной серии.
3.5 Запись в таблицу 1 величины главного квантового числа n 0 для нижнего уровня энергии данной серии, названия серии и длины волн отдельных линий.
3.4 Вычисление и запись в таблицу 1 обратных длин волн.
3.5 Определите, переходу между какими квантовыми состояниями электрона в атоме водорода соответствует каждая линия излучения. Запись в таблицу значения n.
3.6 Построение графика зависимости обратной длины волны (1/l) от обратного квадрата главного квантового числа (1/n 2) для данной спектральной серии.
3.7 Определение по наклону графика значение постоянной Ридберга
3.8 Оформление отчета.
4 Краткие теоретические сведения
4.1 Открытие сложного строения атома - важнейший этап становления современной физики, наложивший отпечаток на все ее дальнейшее развитие. В процессе создания количественной теории строения атома, позволившей объяснить атомные спектры, были открыты новые законы движения микрочастиц - законы квантовой механики.
Английский физик Эрнест Резерфорд исследовал рассеяние a-частиц веществом и открыл в 1911г. атомное ядро - массивное образование, в несколько тысяч раз меньшее по размеру, чем атом.
4.2 Модель Томсона. Не сразу ученые пришли к правильным представлениям о строении атома. Первая модель атома была предложена английским физиком Дж. Дж. Томсоном, открывшим электрон. По мысли Томсона, положительный заряд атома занимает весь объем атома и распределен в этом объеме с постоянной плотностью. Простейший атом - атом водорода - представляет собой положительно заряженный шар радиусом около 10 -8 см, внутри которого находится электрон. У более сложных атомов в положительно заряженном шаре находится несколько электронов, так что атом подобен кексу, в котором роль изюминок играют электроны.
Однако модель атома Томсона оказалась в полном противоречии с опытами по исследованию распределения положительного заряда в атоме. Эти опыты, произведённые впервые Э. Резерфордом, сыграли решающую роль в понимании строения атома.
4.3 Опыты Резерфорда Масса электрона в несколько тысяч раз меньше массы атомов. Так как атом в целом нейтрален, то, следовательно, основная масса атома приходится на его положительно заряженную часть.
Для экспериментального исследования распределения положительного заряда, а значит, и массы внутри атома Резерфорд предложил в 1906 г. применить зондирование атома с помощью a-частиц. Эти частицы возникают при распаде радия и некоторых других элементов. Их масса примерно в 8000 раз больше массы электрона, а положительный заряд равен по модулю удвоенному заряду электрона. Это не что иное, как ионизированные атомы гелия. Скорость a-частиц очень велика:онасоставляет 1/15 скорости света.
Этими частицами Резерфорд бомбардировал атомы тяжелых элементов. Электроны вследствие своей малой массы не могут заметно изменить траекторию a-частицы, подобно тому как камушек в несколько десятков граммов при столкновении с автомобилемне в состоянии заметно изменить его скорость.
Рассеяние (изменение направления движения) a-частиц может вызвать только положительно заряженная часть атома. Таким образом, по рассеянию a-частиц можно определить характер распределения положительного заряда и массы внутри атома. Схема опытов Резерфорда показана на рисунке 1 .

1 Свинцовый цилиндр с источником a-частиц
2 Тонкая фольга
3 Экран с люминофором
4 Микроскоп
Рисунок 1
Радиоактивный препарат, например радий, помещался внутрь свинцового цилиндра 1, вдоль которого был высверлен узкий канал. Пучок a-частиц из канала падал на тонкую фольгу 2 из исследуемого материала (Золото, медь и пр.). Послерассеяния a-частицы попадали на полупрозрачный экран 3, покрытый сульфидом цинка. Столкновение каждой частицы с экраном сопровождалось вспышкой света (сцинтилляцией), которую можно было наблюдать в микроскоп 4. Весь прибор размещался в сосуде, из которого был откачан воздух.
При хорошем вакууме внутри прибора в отсутствие фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком a-частиц. Но когда на пути пучка помещали фольгу, a-частицы из-за рассеяния распределялись на экране по кружку большей площади.
Модифицируя экспериментальную установку, Резерфорд попытался обнаружить отклонение a-частиц на большие углы. Совершенно неожиданно оказалось, что небольшое число a-частиц (примерно одна из двух тысяч) отклонилось на углы, большие 90°.
4.4 Определение размеров атомного ядра. Резерфорд понял, что a-частица могла быть отброшена назад лишь в том случае, если положительный заряд атома и его масса сконцентрированы в очень малой области пространства. Так Резерфорд пришел к идее атомного ядра - тела малых размеров, в котором, сконцентрированы почти вся масса и весь положительный заряд атома.
На рисунке 2,а показаны траектории a-частиц, пролетающих на различных расстояниях от ядра.

Рисунок 2 а) и б)
Подсчитывая число a-частицы, рассеянных на различные углы, Резерфорд смог оценить размеры ядра. Оказалось, что ядро имеет диаметр порядка 10 -12 -10 -13 см (у разных ядер диаметры различны). Размер же самого атома 10 -8 см, т.е. в 10-100 тыс. раз превышает размеры ядра. Впоследствии удалось определить и заряд ядра. При условии, что заряд электрона принят за единицу, заряд ядра в точности равен номеру данного химического элемента в периодической системе Д. И. Менделеева.
4.5 Планетарная модель атома. Из опытов Резерфорда непосредственно вытекает планетарная модель атома. В центре расположено положительно заряженное атомное ядро, в котором сосредоточена почти вся масса атома. В целом атом нейтрален. Поэтому число внутриатомных электронов, как и заряд ядра, равно порядковому номеру элемента в периодической системе. Ясно, что покоиться электроны внутри атома не могут, так как они упали бы на ядро. Они движутся вокруг ядра, подобно тому, как планеты обращаются вокруг Солнца. Такой характер движения электронов определяется действием кулоновских сил со стороны ядра.
В атоме водорода вокруг ядра обращается всего лишь один электрон. Ядро атома водорода имеет положительный заряд, равный по модулю заряду электрона, и массу, примерно в 1836,1 раза большую массы электрона. Это ядро было названо протоном и стало рассматриваться как элементарная частица. Размер атома - это радиус орбиты его электрона (рисунок 2 б).

Рисунок 3 Планетарная модель атома
Простая и наглядная планетарная модель атома имеет прямое экспериментальное обоснование. Она кажется совершенно необходимой для объяснения опытов по рассеиванию a-частицы. Но на основе этой модели нельзя объяснить факт существования атома, его устойчивость. Ведь движение электронов по орбитам происходит с ускорением, причем весьма немалым. Ускоренно движущийся заряд по законам электродинамики Максвелла должен излучать электромагнитные волны с частотой, равной частоте его обращения вокруг ядра Излучение сопровождается потерей энергии. Теряя энергию, электроны должны приближаться к ядру, подобно тому, как спутник приближается к Земле при торможении в верхних слоях атмосферы. Как показывают строгие расчеты, основанные на механике Ньютона и электродинамике Максвелла, электрон за ничтожно малое время (порядка 10 8 с) должен упасть на ядро Атом должен прекратить свое существование.
В действительности ничего подобного не происходит. Атомы устойчивы и в невозбужденном состоянии могут существовать неограниченно долго, совершенно не излучая электромагнитные волны.
Не согласующийся с опытом вывод о неизбежной гибели атома вследствие потери энергии на излучение - это результат применения законов классической физики к явлениям, происходящим внутри атома. Отсюда следует, что к явлениям атомных масштабов законы классической физики неприменимы. Резерфорд создал планетарную модель атома: электроны обращаются вокруг ядра, подобно тому,какпланеты обращаются вокруг Солнца. Эта модель проста, обоснована экспериментально, но не позволяет объяснить устойчивость атомов.
4.6 Спектры. Виды спектров Спектром электромагнитного излучения (ЭМИ) называется совокупность электромагнитных волн, излучаемых или поглощаемых атомами (молекулами) данного вещества.
Все атомы химического элемента обладают одинаковым зарядом атомного ядра, их электронные оболочки имеют одинаковое строение. Поэтому набор частот испускаемых квантов или длин волн излучаемого света у всех атомов одного элемента одинаков.
У каждого химического элемента свой заряд атомного ядра и свое особое строение электронной оболочки. Возбужденные атомы каждого химического элемента испускают световые кванты таких частот, какие не испускают атомы ни одного другого химического элемента. Состав излучения по длинам волн можно узнать, пропустив узкий пучок света через стеклянную призму. Получающийся при разложении линейчатый спектр служит точным «паспортом», по которому можно узнать химический элемент.
Спектры испускания условно делятся на три типа:
а) Светящиеся твердые и жидкие (расплавленные) тела излучают комплексы лучей с постепенным переходом от волн одной длины к волнам другой длины, поэтому спектр их излучения имеет вид цветной полоски с непрерывно изменяющейся окраской, они содержат все длины волн в определенном диапазоне. Такие спектры называются сплошными .
б) Светящиеся атомарные пары и газы (пламя, газы в разрядных трубках) дают спектры прерывистые, или линейчатые, состоящие из отдельных цветных линий, получающиеся от лучей с разными длинами волн. Линейчатый спектр состоит из отдельных компонент (линий), близких к гармоническим. Расстояние между линиями (по шкале длин волн или частот) много больше ширины линий.
в) Полосатые спектры , состоят из совокупности нескольких полос испускания, разделенных промежутками; такие спектры характерны для разреженных молекулярных газов.
Всякое вещество способно поглощать часть проходящего через него излучения. Если через вещество пропускается свет с непрерывным спектром, то спектральный анализ прошедшего света показывает, что в исходно непрерывном спектре появляются отдельные темные линии (спектр поглощения). Спектры солнечного излучения основной массы Солнца имеет вид сплошного, но с большим числом темных тонких линий, пресекающих спектр, получающихся от излучения раскаленных паров и газов, окружающих в виде оболочки основную массу Солнца и поглощающих те лучи, которые они сами испускают. Так как яркость испускания газов солнечной оболочки гораздо меньше, чем яркость лучей основного ядра, то соответственные места спектра кажутся темными. Главные лучи поглощения солнечного спектра называются фраунгоферовыми и отмечаются буквами латинского алфавита.
Г. Кирхгоф установил, что атомы или молекулы данного вещества поглощают свет тех же длин волн, которые они сами могут испускать. Таким образом, положение ярких линий в спектре испускания данного вещества в точности соответствует положению темных линий в спектре поглощения этого же вещества.
Атомы или молекулы каждого вещества, как отмечалось выше, испускают спектр строго определенных частот, являющийся однозначной характеристикой самого вещества. Таким образом, спектральный анализ (т.е. изучение спектра испускания данного вещества) позволяет безошибочно определить химический состав вещества. Спектральный анализ имеет широчайшие применения в технике и других областях (например, криминалистике).
Важнейшую роль играют исследования спектров испускания далеких звезд, позволяющие установить химический состав верхних слоев звезды, распространенность тех или иных элементов, как в самих звездах, так и в межзвездном пространстве. Кроме того, сдвиг положения спектральных линий, связанный с эффектом Доплера, позволяет точно измерить скорость удаления или приближения к нам звезды или галактики, несмотря на колоссальные расстояния до этих объектов.
4.7 Модель Бора Описанная планетарная модель атома совершенно неприемлема с точки зрения законов классической физики. Дело в том, что, как вытекает из законов электродинамики Максвелла, любой ускоренно движущийся заряд излучает электромагнитные волны. Поэтому электрон, двигаясь с центростремительным ускорением υ 2 /r по орбите, постепенно должен терять энергию и неизбежно упасть на ядро. Можно подсчитать время жизни атома водорода до момента падения электрона на ядро. Оказывается, что атом просуществовал бы всего около 10 -10 с.
В 1913 г. Н. Бор предложил теоретическое объяснение модели атома Резерфорда, основанное на отказе от ряда классических представлений, прежде всего, на отказе от утверждения о непрерывности классических величин типа энергии и момента импульса. Этим Бор заложил основы квантовой теории.
В дальнейшем полуклассическая и во многом непоследовательная модель Бора была заменена строгими законами квантовой механики.
4.8 Постулаты Бора:
1. Электрон в атоме водорода может находиться только на орбитах, для которых значение момента импульса электрона в единицах ħ= h/2π =1,0545·10 -34 Дж·с равно целому числу:
L = mυr n = n(h/2π) =nħ, (1)
где L - момент импульса электрона, m - его масса, r n - радиус n-ой орбиты, h=6,626·10 -34 Дж·с, n = 1, 2, 3, ...
Соответственно энергия электрона на каждой из орбит имеет определенное значение E n , а другие значения энергии невозможны.
2. Находясь на этих орбитах, электрон не излучает энергию.
3. Излучение энергии в виде электромагнитного излучения происходит только при переходе (скачке) электрона с одной орбиты (с большей энергией E n) на другую (с меньшей энергией E m), причем энергия испущенного фотона
hν = E n - E m . (2)
С помощью этих постулатов можно вычислить радиусы разрешенных орбит и энергию электрона на них для атома водорода. Используем два уравнения:
постулат Бора: mυr n =ħn; (3)
закон движения: mυ 2 /r n = ke 2 /r n 2 . (4)
Исключая υ из нижнего соотношения с помощью верхнего, получим:
![]() (5)
(5)
где ε 0 =8,854·10 -12 Ф м -1 - электрическая постоянная, е = 1,6022 10 -19 Кл - заряд электрона, n=1, 2, 3, ...
Пользуясь формулой, связывающей полную энергию с потенциальной, находим разрешенные значения энергии для атома водорода:
![]() , где n=1, 2, 3, ... (6)
, где n=1, 2, 3, ... (6)
При n = 1 получаются наименьшее возможное значение радиуса орбиты a = r 1 (боровский радиус) и наибольшее по абсолютной величине значение полной энергии электрона E 1 = - ke 2 /(2a). Говорят, что в этом случае электрон находится в основном состоянии.
Численно a = = 0,53·10 -10 м =0,053 нм; (7)
Е 1 =  = - 2,17·10 -18 Дж = - 13,6 эВ. (8)
= - 2,17·10 -18 Дж = - 13,6 эВ. (8)
Здесь введена принятая в задачах атомной и ядерной физики единица измерения энергии - электрон-вольт (эВ) - равная работе по перемещению элементарного заряда е между точками с разностью потенциалов ΔU = 1 В:
1 эВ = eΔU = 1,6 10 -19 Кл·1 В = 1,6·10 -19 Дж.
Пользуясь постулатом Бора, можно также вычислить импульс и скорость электрона на первой боровской орбите:
р 1 = ħ/a=  = αmc » mc/137=0,2×10 -23 м/с (9)
= αmc » mc/137=0,2×10 -23 м/с (9)
υ 1 = р 1 /m = αс » c/137=2,2×10 6 м/с. (10)
Здесь введена важная безразмерная фундаментальная постоянная, определяющая интенсивность электромагнитного взаимодействия:
α = » 1/137 (11)
Она называется постоянной тонкой структуры.
Радиусы других орбит даются формулой:
r n = α·n 2 , n = 1, 2, 3, ... (12)
Электрон может находиться в любом из состояний с энергией, которая определяется формулой:
E n = E 1 /n 2 , n = 1, 2, 3, ... (13)
Эти состояния называются стационарными состояниями. Находясь в стационарном состоянии, электрон не излучает энергию.
Излучение в форме фотонов - квантов света - происходит при переходе электрона из состояния с большим значением энергии Е n в любое из состояний с меньшим значением энергии E m . При таком переходе испускается фотон с энергией hν, определяемой по закону сохранения энергии:
hν = E n - E m . (14)
Если перейти к длинам волн фотонов, используя соотношение ν=c/λ, то после подстановки значений энергии получим:
![]() = = (15)
= = (15)
Введенная здесь постоянная R y = 1,097·10 7 м -1 называется постоянной Ридберга.
Спектральные серии водорода, наблюдаемые на опыте, соответствуют переходам из возбужденных состояний с номерами m в конечные состояния с номерами n = 1, 2, 3, ...:
![]() m= 2, 3, 4, ¼. (16)
m= 2, 3, 4, ¼. (16)
(серия Лаймана);
![]() , m= 3, 4, 5, ¼. (17)
, m= 3, 4, 5, ¼. (17)
(серия Бальмера);
![]() , m= 4, 5, 6,¼. (18)
, m= 4, 5, 6,¼. (18)
(серия Пашена) и т.д.
Следует отметить, что представление о движении электрона в атоме по законам классической механики по избранным (стационарным) орбитам имеет лишь историческое значение. Современная квантовая физика описывает состояние электрона в атоме с помощью так называемых волновых функций и отказывается от классических представлений о траекториях движения микрообъектов.
4.9 Серия Бальмера водорода Спектры испускания атомов могут быть экспериментально исследованы с помощью приборов, называемых спектроскопами или спектрографами. В простейшем спектроскопе свет проходит через щель и затем разлагается в спектр с помощью призмы. Система линз фокусирует изображение спектра либо для визуального наблюдения либо для записи на фотопластинке. Каждая длина волны света формирует изображение входной щели. Школьный спектроскоп (рисунок 4) состоит из двух труб – коллиматорной 1 и зрительной, укрепленных на подставке 2 , стеклянной призмы 3 под крышкой и микрометрического винта 5 .На одном конце коллиматорной трубы имеется щель для выделения узкого пучка света. На другом её конце – линза для превращения расходящегося пучка света в параллельный пучок. Параллельный пучок света,выходящий из коллиматорной трубы О, падает на грань стеклянной призмы. Коэффициент преломления света зависит от его длины волны, поэтому свет сложного состава разлагается призмой на несколько параллельных пучков и создает цветные изображения щели. (рисунок 5). Эти разноцветные изображения щели и являются линейчатым спектром химического элемента. Измерив длины волн линий полученного спектра и сравнив найденные значения с табличными сведениями о спектрах различных химических элементов, можно узнать, какому элементу принадлежит исследуемый спектр.

Рисунок 4 Школьный спектроскоп
![]()
Рисунок 5 Ход лучей в спектроскопе
Для изучения химического состава вещества методом спектрального анализа исследуемое вещество нагревается до такой температуры, при которой оно находится в газообразном состоянии и излучает свет. Для возбуждения атомов вещества, находящегося в газообразном состоянии, часто используется электрический разряд.
Как уже было выше отмечено, спектры газов содержат серии спектральных линий. Каждая линия соответствует определенной длине волны света, испущенного атомами газа.
Происхождение линейчатых спектров можно объяснить на основе двух концепций. Первая из них - это представление о фотонах; вторая - это концепция энергетических уровней атома. Эти представления были объединены в квантовой теории атома, созданной датским физиком Нильсом Бором в 1913 г.
СПЕКТРАЛЬНОЙ СЕРИЕЙ называется совокупность линий излучения, соответствующих переходу электрона в атоме на один и тот же нижний уровень энергии.
РАДИОЛИНИЯ ВОДОРОДА
21 см - спектральная
линия с длиной волны l ! 21,1 см, обусловленная переходами между
подуровнями сверхтонкой структуры
осн. уровня энергии атома водорода.
Причиной сверхтонкого расщепления является взаимодействие спинов ядра
и электрона. Энергия атома при параллельном расположении спинов несколько больше,
чем при антипараллельном. При изменении ориентации спина электрона на противоположную
происходит испускание (или поглощение) кванта с l ! 21,1
см (частота v ! 1420 МГц). Принципиальная возможность излучения межзвёздным
водородом Р. в. 21 см указана в 1945 X. К. ван де Хюлстом (Н. Ch. van de Hulst).
В 1948 И. С. Шкловский рассчитал ожидаемую интенсивность радиолинии и показал,
что она достаточна для того, чтобы Р. в. 21 см можно было обнаружить методами
радиоастрономии. В каждом отд. атоме переход, рождающий квант радиоизлучения,
происходит в ср. 1 раз за 11 млн. лет, но благодаря высокой распространённости
атомарного водорода в межзвёздной среде радиолиния оказывается достаточно интенсивной.
Р. в. 21 см обнаружена в 1951 почти од-новрем. X. Юэном (Н. Ewen), Э. Пёрселлом
(Е. Pur-cell), К. Мюллером (С. Muller), Я. Оортом (J. Oort).
Р. в. 21 см оказалась эфф. средством исследования
Вселенной. Ок. половины массы галактич. межзвёздного вещества составляет атомарный
водород, находящийся в осн. состоянии. Его можно исследовать только по излучению
Р. в. 21 см; никаким др. образом эта важнейшая составная часть космич. вещества
себя не проявляет. Поэтому Р. в. 21 см даёт ценные, часто уникальные сведения
о строении и распределении материи в космич. пространстве.
Интенсивность Р. в. 21 см содержит непосредств. информацию о числе атомов нейтрального водорода на луче зрения (за исключением направлений на нек-рые плотные облака, центр и антицентр Галактики, в к-рых межзвёздный газ непрозрачен в этой линии), а частота и профиль линии позволяют определить по эффекту Доплера лучевые скорости u R водорода. В соответствии С моделью дифференц. вращения Галактики эти данные дают возможность определить расстояние до излучающих объектов, т. е. найти распределение нейтрального водорода. Исследования Р. в. 21 см позволили установить, что нейтральный водород в Галактике в осн. заключён в очень тонком (! 220 пк) и ровном слое около её плоскости. Лишь на периферии на расстояниях, превышающих 10-12 кпк от центра Галактики, слой водорода размывается до 1000 пк по толщине и отклоняется от галактич. плоскости. В распределении водорода довольно отчётливо выделяются спиральные рукава, к-рые прослеживаются до больших расстояний. На рис. приведён профиль Р. в. 21 см в направлении области Лебедь X (a=20 h 28 m , d = 42°). Отчётливо видны максимумы излучения, соответствующие отд. спиральным рукавам. Наиб. интенсивный максимум при= 3 км/с соответствует ближайшему к Солнцу т. н. Орионову рукаву, максимум при u R = 40 км/с - Персееву рукаву. Внутри рукавов нейтральный водород распределён неравномерно, в них выделяются вытянутые вдоль плоскости Галактики комплексы облаков с характерными размерами ж 200 X X 50 пк. Получены данные о зависимости ср. концентрации нейтрального водорода от галактоцентрич. расстояния и о детальном распределении водорода в отд. галактич. областях, в т. ч. в галактическом центре .
Профиль радиолинии l = 21 см в направлении
области Лебедь X. По оси абсцисс отложена лучевая скорость (),
по оси ординат - линии (Т b).
![]()
Излучение Р. в. 21 см наблюдалось также от большого
числа др. галактик, что позволило установить отношение массы нейтрального водорода
к общей массе галактики в зависимости от её типа. Доля нейтрального водорода
увеличивается при переходе от галактик типа Sа к неправильным, достигая для
последних десятков процентов. Мин. кол-во нейтрального водорода найдено у эллиптич.
галактик; для подавляющего большинства из них доля нейтрального водорода по
массе составляет ~0,1%. Для ряда ближайших галактик по Р. в. 21 см получены
распределения нейтрального водорода в них и кривые вращения (см. Вращение
галактик)
. Ценные данные получены также по красному смещению
Р. в.
21 см. Линия зарегистрирована более чем от 100 галактик, изменение частоты линии
соответствует удалению галактик с разл. скоростями (до ~10 4 км/с)
при хорошей корреляции с красным смещением оптич. линий. Линия водорода, обнаруженная
в спектре удалённого внегалактич. источника - квазара ЗС 286, оказалась смещённой
с частоты 1420,4 МГц до 839,4 Мгц, что соответствует красному смещению г = 0,692.
Полученные данные существенно способствовали развитию теории расширения Вселенной.
Обнаруженная в межзвёздной среде и ставшая эфф. средством исследования космич. пространства Р. в. 21 см нашла также важное земное применение. На её основе разработаны т. н. активные квантовые стандарты частоты . Для создания достаточной интенсивности Р. в. 21 см в земных условиях используют вынужденное испускание фотонов атомами водорода. Из источника, в к-ром под влиянием электрич. разряда при низком давлении происходит диссоциация молекулярного водорода, вылетает пучок атомов водорода. В сортирующем устройстве с помощью магн. поля происходит сортировка атомов: возбуждённые атомы поступают в кварцевую камеру, находящуюся в объёмном


